Deel dit project
Remodeling the Cancer Landscape
Samenvatting
Dit proefschrift onderzoekt de complexe rol van de epigenetica in het aansturen van fenotypische plasticiteit binnen darm- en mondkanker. Er wordt met name onderzocht hoe chromatine-remodelers en microRNA's kankerprogressie en metastase beïnvloeden, door de algemene mechanismen die ten grondslag liggen aan fenotypische plasticiteit in darmkanker te verbinden met een gedetailleerde analyse van de rol van het CDK2APN-gen in het moduleren van de competitieve wisselwerking tussen SWI/SNF- en NuRD-chromatineremodelercomplexen in plaveiselcelcarcinoom van de mond (OSCC).
Hoofdstuk 2 verkent fenotypische plasticiteit, een kerneigenschap van carcinoomcellen die hen in staat stelt hun morfologische en functionele kenmerken aan te passen tijdens lokale invasie en metastase. Dit hoofdstuk onthult een quasi-mesenchymale subpopulatie van darmkankercellen, aangeduid als EpCAMlaag. Deze populatie wordt gekenmerkt door verhoogde mobiliteit, invasiviteit, chemotherapieresistentie en een hoog metastatisch potentieel. Door het uitvoeren van uitgebreide bulk- en single-cell RNA-sequencing, toont de studie verhoogde Wnt/β-catenine-signalering en verschillende gradaties van epitheliale naar mesenchymale transitie (EMT) aan, waaronder hybride E/M-fasen. Deze bevindingen zijn met name belangrijk omdat ze een verband aantonen met het CMS4-subtype, dat bekend staat om de slechte prognose en prominente stromale kenmerken.
In Hoofdstuk 3 breiden we de analyse uit met een andere subpopulatie van epitheliale cellen binnen de SW48O darmkankercellijn. De identificatie van verschillende subpopulaties, namelijk residentiële kankerstamcellen (rCSCs), migrerende CSCs (mCSCs) en cellen verantwoordelijk voor terugval (HRCs) binnen dezelfde darmkankercellijn, benadrukt het belang van heterogeniteit binnen de tumor en de diverse rollen van deze verschillende cellulaire componenten in de dynamiek van de tumor. Spatial transcriptomics data van tumoren van patiënten bevestigen de aanwezigheid en de specifieke verspreiding van deze subpopulaties, wat ons begrip van hun impact op de tumor versterkt.
Hoofdstuk 4 maakt een transitie van darmkanker naar mondkanker. Dit hoofdstuk richt zich op de repressie van het CDK2APN tumorsuppressorgen in OSCC, dat codeert voor een belangrijk component van het NuRD-complex. De centrale onderzoeksvraag in dit hoofdstuk was hoe het mogelijk is dat, ondanks de lage frequentie van mutaties in zijn coderende sequentie, het CDK2APN-gen vaak lager tot expressie komt bij mondkanker. Tijdens dit onderzoek hebben we verschillende microRNA's geïdentificeerd die de translatie van CDK2APN remmen, en hebben we een nieuwe gecombineerde ISH/IF-techniek ontwikkeld om de expressie in de context van de histologie van plaveiselceltumoren te analyseren. Bovendien blijkt de epigenetische regulatie van de nieuw geïdentificeerde microRNA's van significante invloed op overleving van patiënten, waardoor het klinische belang van epigenetische controle in OSCC wordt benadrukt.
Hoofdstuk 5 voegt meer complexiteit toe door de tweeledige rollen van fenotypische plasticiteit en ontsteking bij kankerprogressie te onderzoeken, en richt zich op hun regulatie door de competitieve dynamiek tussen de NuRD- en SWI/SNF-chromatineremodelercomplexen in OSCC. Hier laten we zien hoe verstoringen van deze eiwitcomplexen ontsteking signaaltransductiepaden en epitheliaal-mesenchymale plasticiteit beïnvloeden. In het bijzonder toon ik aan dat het verlies van CDK2APN een pro-inflammatoir secretoom versterkt, waardoor monocyten worden aangetrokken die zich differentiëren tot M2-achtige macrofagen binnen de tumormicro-omgeving. Deze bevindingen slaan niet alleen een brug tussen chromatine remodeling en ontstekingsreacties en EMP, maar suggereren ook de mogelijkheid om CDK2APN en gerelateerde chromatine remodelers te gebruiken zowel als prognostische markers als voor therapeutische doeleinden.
Hoofdstuk 6 brengt ten slotte de inzichten uit beide kankertypes samen en bespreekt innovatieve strategieën om de complexiteit van de verschillende chromatineremodelers in de context van fenotypische plasticiteit bij kanker te ontcijferen. Dit hoofdstuk behandelt de uitdagingen en mogelijkheden van het bestuderen van epigenetische mechanismen die aan deze plasticiteit ten grondslag liggen. Daarbij worden nieuwe benaderingen voor kankertherapie voorgesteld die gebruikmaken van ons begrip van chromatinedynamiek en microRNA-regulatie. Door deze bevindingen te integreren, stelt het proefschrift een nieuw kader voor de behandeling van kanker voor, met de nadruk op de mogelijkheid om de epigenetische interacties te ontwrichten die bijdragen aan de flexibiliteit en weerbaarheid van kankercellen.
Bekijk ook deze proefschriften
Structure-Preserving Data-Driven Methods for Modeling Turbulent Flows
Molecular insights into the role of VRS5 in tillering and lateral spikelet development in barley
Gamma Knife Radiosurgery for Skull Base Tumors
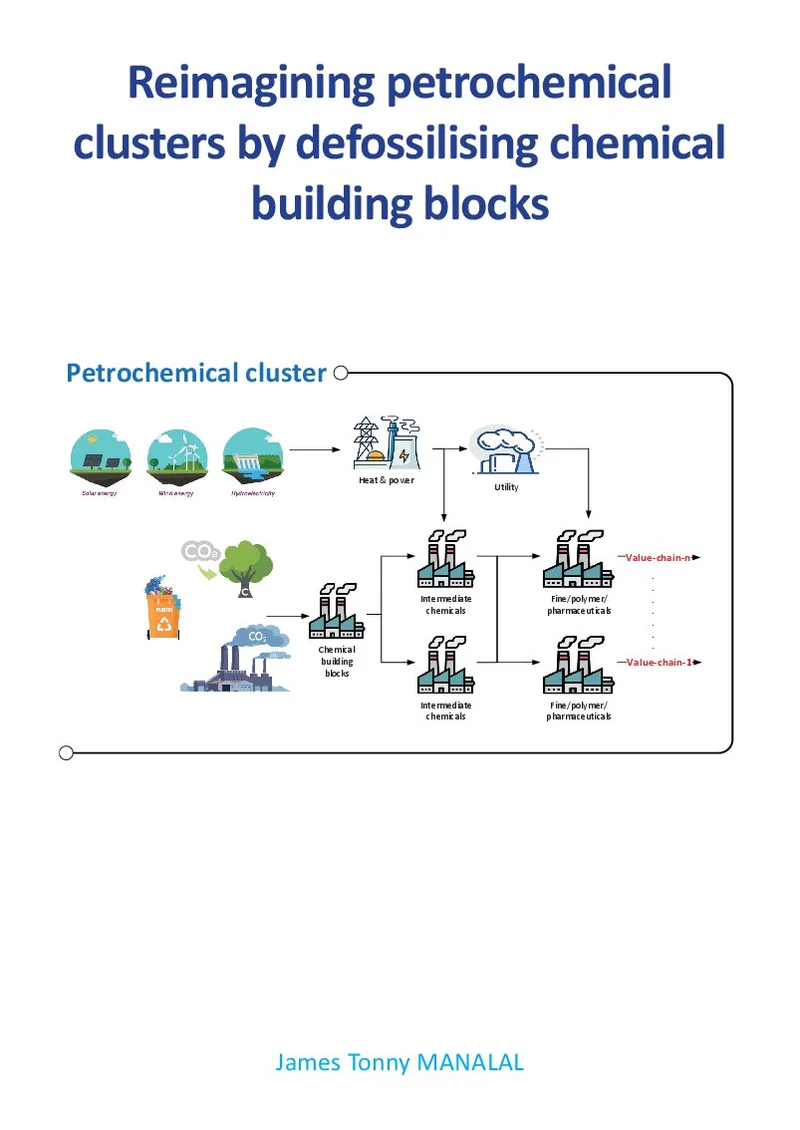
Reimagining petrochemical clusters by defossilising chemical building blocks
Microbial stabilization and protein functionality of plant-based liquids using pulsed electric fields
Wij drukken voor de volgende universiteiten