Deel dit project
Adipose tissue dysfunction and cardiometabolic risk
Samenvatting
Een goed functionerend lichaam kan niet zonder vetweefsel. Zonder dit weefsel raken diverse lichaamssystemen ontregeld, waaronder de opslag van vetten, de glucosehuishouding en tal van hormonale processen. Goed functionerend vetweefsel beschermt tegen het ontstaan van diabetes, metabool syndroom en uiteindelijk hart- en vaatziekten. Vetweefsel wordt dus niet langer beschouwd als orgaan wat alleen vet opslaat, maar als een belangrijk endocrien orgaan. Echter, een teveel aan vetweefsel door overmatige vetzucht (obesitas) kan zorgen voor ontregeling van deze metabole processen. Het vet raakt dan dysfunctioneel. Het aantal mensen met obesitas is de laatste jaren enorm gegroeid, waardoor wordt gesproken van een obesitas-epidemie. Tegenwoordig overlijden zelfs meer mensen aan de gevolgen van overvoeding dan aan de gevolgen van ondervoeding. Het blijkt voor veel mensen moeilijk om de inname van voeding te beperken of om voeding te verbranden. Daarom moeten we op zoek naar manieren om tekenen van dysfunctionerend vet vroegtijdig te signaleren (voor diagnostische doeleinden) en te behandelen (voor therapeutische doeleinden). Hiervoor is begrip van de biologische processen die leiden tot cardiometabole ziekten als gevolg van dysfunctionerend vet essentieel. Echter, terwijl de obesitas-epidemie zich in een alarmerend tempo ontwikkelt zijn we wetenschappelijk gezien nog steeds ver achter met de ontwikkeling van diagnostische en therapeutische middelen.
In dit proefschrift hebben we vetweefsel en de gevolgen van vetweefseldysfunctie op drie niveaus bestudeerd: middels klinische studies, analyse van gekweekte vetcellen (in vitro) en analyse van menselijke vetweefselbiopten (ex vivo). Hierbinnen presenteren we een nieuw mechanisme in obesitas-geïnduceerde comorbiditeit: de rol van extracellulaire membraanblaasjes.
In hoofdstuk 1 wordt de endocriene rol van vetweefsel geïntroduceerd. Vetweefsel communiceert met andere organen door middel van uitscheiding van vetcel specifieke eiwitten (adipokines) en vrije vetzuren, maar ook door middel van extracellulaire membraanblaasjes. Deze kleine blaasjes worden in de (vet)cel gevormd en, door versmelting met het celmembraan, uitgescheiden in de extracellulaire ruimte. Extracellulaire membraanblaasjes zijn cruciaal in de communicatie tussen cellen in ons lichaam. Ze vervoeren meerdere moleculen tegelijk, zoals talloze lipiden, eiwitten en genetisch materiaal, waarmee de blaasjes cellen van andere organen kan activeren. Deze eigenschappen maken membraanblaasjes interessante kandidaten voor diagnostische en therapeutische doeleinden. Zo kunnen membraanblaasjes belangrijk zijn voor de ontwikkeling van medicijnen, omdat ze een essentiële rol spelen in de communicatie tussen vetcellen en andere cellen die betrokken zijn bij vetweefseldysfunctie. Ten tweede kunnen membraanblaasjes afkomstig van vetweefsel iets vertellen over de staat van de dysfunctie van het vet. Hierdoor kunnen we mogelijk het risico van een patiënt met obesitas beter kunnen monitoren.
In hoofdstuk 2 wordt de huidige kennis over de onderliggende mechanismen van obesitas en metabole dysfunctie besproken, met een speciale focus op verschillende vetweefselgebieden en de rol van het vetweefsel afkomstige membraanblaasjes. Vetcellen vervullen een belangrijke taak in de opslag van vetten (triglyceriden), maar ook is er een limiet in de hoeveelheid vetten die een vetcel kan opslaan. In het geval van overmatige vetzucht (obesitas) is er een langdurig te hoog aanbod van energie die moet worden opgeslagen. Die opslag kan in bestaande vetcellen die gaan uitzetten (hypertrofie) of in nieuw aangemaakte vetcellen (hyperplasie). Als beide opslagmogelijkheden in vetweefsel verzadigd zijn (een grens die bij ieder persoon anders is), wordt de ingenomen energie noodgedwongen in andere organen zoals de lever of in de bloedvaten opgeslagen. Dit zorgt voor een verstoring van de functie van deze andere organen, zoals de leverfalen en vernauwing van de bloedvaten. Daarnaast raken de andere functies van de oververzadigde vetcellen verstoord. Dit wordt vetweefseldysfunctie genoemd. Een gezonde vetcel is gevoelig voor het hormoon insuline, waardoor glucose uit de bloedbaan opgenomen kan worden voor tijden waarin energie nodig is. Dysfunctionerende vetcellen zijn niet langer gevoelig voor insuline (insulineresistentie), met als gevolg dat de bloedglucose stijgt. Dit kan uiteindelijk leiden tot suikerziekte (diabetes). Tot slot produceert gezond vet tal van hormonen en eiwitten (collectief adipokines genoemd), zoals het hongerhormoon leptine en het anti-diabetische adiponectine. Deze laatste regelt doorcommunicatie met andere organen verschillende processen in het lichaam. Dysfunctioneel vet trekt tal van ontstekingscellen aan zoals macrofagen en T cellen, die samen met de vetcellen tal van ontsteking (pro-inflammatoire) eiwitten uitscheiden zoals interleukines (IL-1, IL-6) tumor necrose factor alfa (TNF-α) en resistine. De verschillende typen pro-inflammatoire eiwitten kunnen zorgen voor ontstekingsreacties en bijdragen aan vaatschade, hypertensie en insuline resistentie. Deze combinatie van risicofactoren wordt het metabool syndroom genoemd. Naast de rol van pro-inflammatoire eiwitten en immuun cellen wordt ook de potentiële rol van membraanblaasjes in de ontwikkeling van obesitas geïnduceerde cardiometabool risico beschreven in dit review.
De verstoring van vetweefsel is verschillend op verschillende plekken in het lichaam. In hoofdstuk 3 hebben we ontstekingseigenschappen van vier verschillende vetweefsel gebieden uit de buik onderzocht. Het vetweefsel onder de huid (subcutaan vetweefsel) wordt beschouwd als gezond vet. De vetcellen van dit type vet zijn in staat tot grotere opslag van vetten, zonder hierbij dysfunctioneel te raken. Daarbij scheiden ze veel metabool gunstige hormonen uit. Het vet rondom organen (visceraal vet) is het ‘ongezonde vet’ omdat het minder capaciteit heeft om te anticiperen op toename van energie aanvoer en daarbij meer ontstekingseiwitten uitscheidt. Echter, de verschillende ontstekingseigenschappen van verschillende viscerale vetweefselregio’s is minder goed bekend. Tijdens een operatie aan de grote buikslagader zijn stukjes van het onderhuidse vetweefsel en drie viscerale vetweefsels verzameld. Karakteristieken van die vier vetstukjes werden vergeleken tussen mannen met en mannen zonder overgewicht. De meest opvallende bevinding was dat verschillende viscerale vetweefsel gebieden gerelateerd zijn aan verschillende kenmerken van het metabool syndroom. Vet rondom de aorta bevat veel ‘crown like structures’ (macrofagen die een doodgaande vetcel opruimen, een teken van vetweefseldysfunctie) en scheidt hoge concentraties adipokines uit, maar de morfologische kenmerken hielden geen verband met systemische metabole dysfunctie. Het vetweefsel tussen de darmen (mesenteriaal vet) en het vetschort (omentum) waren beide wel gerelateerd aan metabole verstoringen. De hoeveelheid ‘crown like structures’ van mesenteriaal vet was hierbij gerelateerd aan insuline resistentie, terwijl ‘crown like structures’ in omentaal vet gerelateerd waren aan hogere triglyceride waarden en lager HDL-cholesterol. Deze resultaten wijzen erop dat verschillende viscerale vetweefsel gebieden anders aan metabole ziekten gerelateerd zijn. Aangezien mesenteriaal vet tussen de darmen ligt, is het interessant om te speculeren over een mogelijk samenspel tussen de darmen en mesenteriaal vet. Wellicht verstoren stoffen die geproduceerd zijn door dysfunctioneel mesenteriaal vet de uitscheiding van insuline stimulerende hormonen van de darm. De bevindingen beschreven in hoofdstuk 3 geeft de noodzaak aan om de potentieel verschillende bijdrage van omentaal en mesenteriaal vet aan obesitas-geïnduceerde metabole stoornissen verder te onderzoeken, zodat specifiekere medicijnen ontwikkeld kunnen worden.
In het tweede deel van dit proefschrift beschrijven we studies over de rol van extracellulaire membraanblaasjes in vetweefsel, vetweefseldysfunctie en insuline resistentie. In hoofdstuk 4 hebben we onderzocht of membraanblaasjes afkomstig van menselijke in vitro gekweekte vetcellen of ex vivo gekweekte vetbiopten een rol kunnen spelen in de activatie van macrofagen. Activatie van macrofagen in dysfunctioneel vetweefsel is cruciaal in de ontwikkeling van insuline resistentie. In dit hoofdstuk hebben wij aangetoond dat membraanblaasjes afkomstig van vet een rol spelen in de paracriene communicatie tussen vetcellen en macrofagen. Membraanblaasjes afkomstig van vet konden macrofagen activeren, die vervolgens insulineresistentie induceerden in in vitro gedifferentieerde vetcellen. Het is nog niet bekend hoe de membraanblaasjes macrofagen precies activeren. Membraanblaasjes kunnen bijvoorbeeld ontstekingseiwitten bevatten die daar een rol in zouden kunnen spelen. Karakterisering van de ontstekingseiwitten aanwezig op membraanblaasjes en afkomstig van vetweefsel, toonde aanwezigheid aan van talrijke adipokines, waaronder ‘macrophage migration inhibitory factor’ (MIF) en adiponectine. Naast een lokaal effect van membraanblaasjes op insuline resistentie, was het aantal membraanblaasjes van visceraal vet (maar niet van het onderhuidse vet) ook gerelateerd aan systemische insulineresistentie. Om de relatie tussen membraanblaasjes afkomstig van vetweefsel en systemische insuline resistentie beter te onderzoeken, hebben we vervolgens bestudeerd of de membraanblaasjes ook kunnen interfereren met de signaalroute van insuline in de lever en spiercellen. Dit is beschreven in hoofdstuk 5. Hierbij toonden we eerst aan dat adiponectine-positieve membraanblaasjes aanwezig zijn in het bloed van mensen. Aangezien adiponectine alleen door vetcellen wordt gemaakt, suggereert deze bevinding dat membraanblaasjes van vetweefsel ook in de bloedsomloop terecht komen, en zo op afstand effect op andere organen kunnen hebben. Vervolgens zagen we dat membraanblaasjes van ex vivo vet biopten rechtstreeks de insuline signaalroute van levercellen kunnen verstoren. Het effect op spiercellen was echter minder duidelijk. Ten slotte bleek dat de mate van insuline resistentie in de levercellen afhankelijk is van de concentraties van ontstekingseiwitten, waaronder MIF en MCP-1. Op basis van deze resultaten concludeerden we dat membraanblaasjes afkomstig van vetweefsel kunnen bijdragen aan insuline-resistentie, zowel lokaal (via activatie van macrofagen) als systemisch (via verstoring van de insuline signaalroute in levercellen). Dit is een nieuw mechanisme waarop vetweefsel bij kan dragen aan metabole stoornissen.
In het laatste deel van dit proefschrift is de relatie tussen vetcel specifieke eiwitten en metabole stoornissen en hart- en vaatziekten in grote patiënten populaties onderzocht. Dysfunctioneel vet kan bijvoorbeeld eiwitten uitscheiden die de mate van vetweefsel-dysfunctie weerspiegelen, en ook het risico op complicaties voorspellen zoals diabetes en hart en vaatziekten. Zulke eiwitten worden dan biomarkers genoemd. Maar ook membraanblaasjes zouden geschikte biomarkers kunnen zijn, wat al voor veel ziektes aangetoond is. Biomarkers voor obesitas-geïnduceerde ziekte zijn echter nog schaars. Een potentieel interessante biomarker is adiponectine. De concentratie van adiponectine in het bloed is verlaagd in mensen met obesitas, en lage adiponectine waardes zijn weer geassocieerd met het ontstaan van diabetes. Aangezien obesitas en diabetes beide belangrijke risicofactoren zijn voor hart en vaatziekten hebben we in hoofdstuk 7 de potentiële prognostische waarde van adiponectine voor hart en vaatziekten bestudeerd. In deze meta-analyse (een studie waarin de onderzoeksresultaten van meerdere studies wordt gecombineerd) blijkt dat de adiponectine waardes van in totaal 23.919 patiënten niet zijn gerelateerd aan het ontstaan van hart en vaatziekten. Deze resultaten impliceren dat ondanks alle gunstige effecten van adiponectine op ontstekingen, de insuline gevoeligheid en de vaatwand die zijn waargenomen in vivo (in muisproeven) of in vitro (in een kweekschaaltje), dit hormoon niet geschikt is als biomarker voor obesitas geïnduceerde hart en vaatziekten. Een verklaring hiervoor kan liggen in het feit dat obesitas geïnduceerde hart en vaatziekten multifactorieel bepaald worden (via meerdere en verschillende manieren), en dat een eiwit wat slechts één van de onderliggende routes weerspiegeld niet voldoende informatie geeft over alle processen die geactiveerd zijn in obesitas en die bijdragen aan diabetes en hart en vaatziekten. Om een goede biomarker voor een complexe ziekte als obesitas te vinden, zullen we dus waarschijnlijk toe moeten naar een multifactorieel signaal, wat te vinden is in membraanblaasjes. Zoals hierboven beschreven bevatten membraanblaasjes meerdere moleculen, zoals adiponectine en tal van andere ontstekingseiwitten en vetten. Wellicht dat de combinatie van meerdere typen moleculen, verpakt in één membraanblaasje, een betere afspiegeling geeft van de ziekte staat van een patiënt. De rol van membraanblaasjes als biomarker voor hart en vaatziekten is al meerdere keren aangetoond, maar de potentie van membraanblaasjes voor metabole stoornissen is een grotendeels onontgonnen gebied. In hoofdstuk 6 hebben we de mogelijkheid van membraanblaasjes als biomarker voor metabole stoornissen onderzocht. Van vier eiwitten, aanwezig in membraanblaasjes uit het bloed, is de relatie met obesitas, het metabool syndroom en het ontstaan van suikerziekte onderzocht in een cohort van 1012 patiënten met hart en vaatziekten. Het eiwit cystatine C op membraanblaasjes was geassocieerd met het hebben van het metabool syndroom en een lager HDL-cholesterol, terwijl CD14 waardes juist verlaagd waren in mannen met obesitas en hogere CD14 geassocieerd met een lagere kans op de ontwikkeling van diabetes type 2. Uit deze resultaten blijkt dat eiwitten van membraanblaasjes als biomarker zouden kunnen fungeren voor obesitas-geïnduceerde diabetes.
Een beter begrip van de onderliggende mechanismen waarop obesitas kan leiden tot diabetes en hart en vaatziekten zal ons moeten helpen in de ontwikkeling van de juiste medicijnen. De huidige kennis wijst op een multifactorieel en onderling afhankelijk proces, waarin naast lagere hoeveelheid hormonen die gunstig zijn voor je stofwisseling, talrijke andere moleculen juist worden geactiveerd zoals ontstekingseiwitten en vrije vetzuren. Een dergelijk complexe ziekte vraagt om een multifactoriële aanpak die kan worden gevonden in membraanblaasjes. Karakterisering van de samenstelling van vetweefselblaasjes zou ons in staat stellen om een multi-parameter biomarker te ontwikkelen voor obesitas geïnduceerde ziekte. Daarnaast zou manipulatie van de inhoud en de bindingscapaciteit van vetweefsel-membraanblaasjes aan andere cellen therapeutische potentie kunnen hebben.
Bekijk ook deze proefschriften
Structure-Preserving Data-Driven Methods for Modeling Turbulent Flows
Molecular insights into the role of VRS5 in tillering and lateral spikelet development in barley
Gamma Knife Radiosurgery for Skull Base Tumors
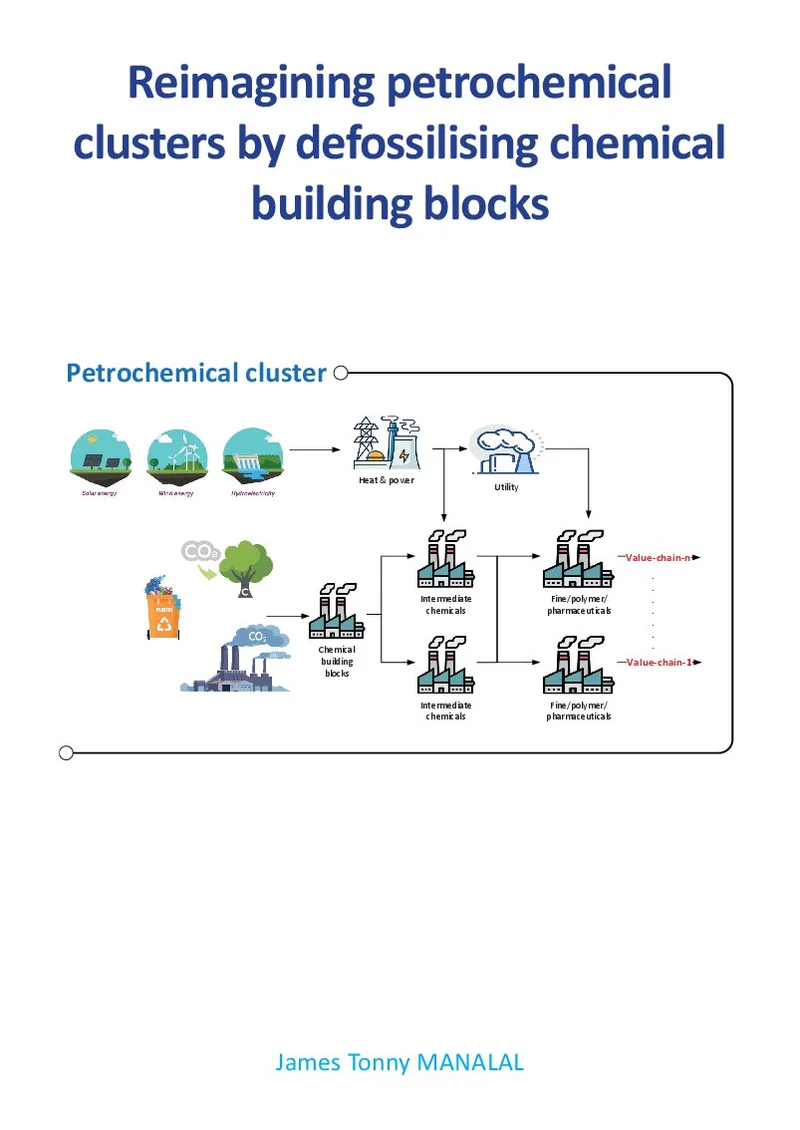
Reimagining petrochemical clusters by defossilising chemical building blocks
Microbial stabilization and protein functionality of plant-based liquids using pulsed electric fields
Wij drukken voor de volgende universiteiten