Deel dit project
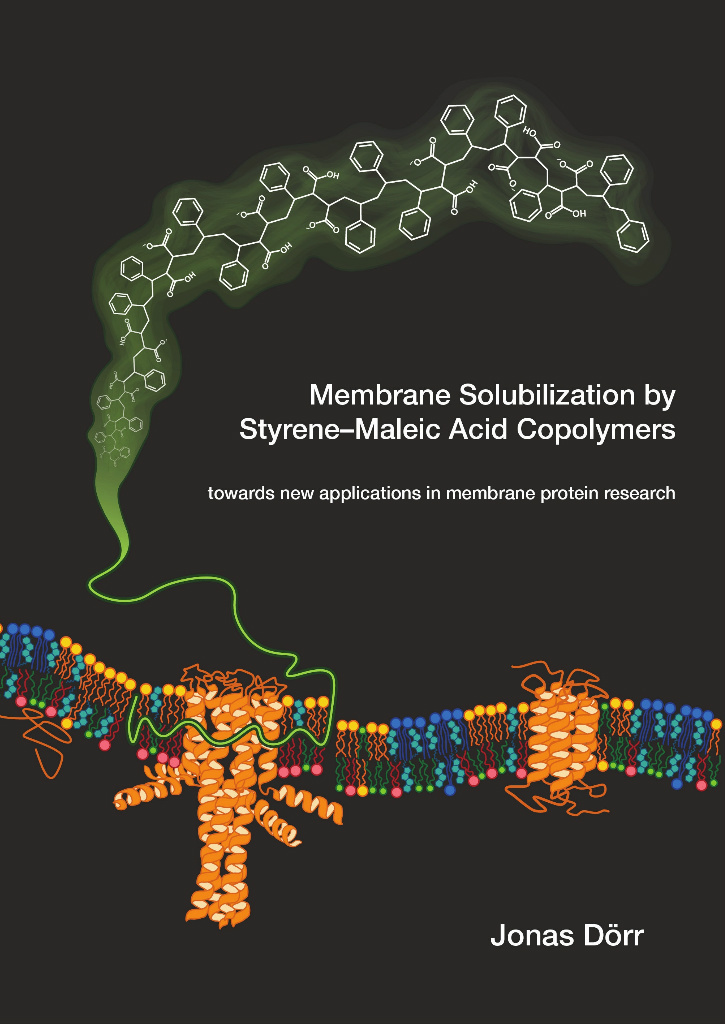
Membrane solubilization by styrene–maleic acid copolymers
Samenvatting
Deze van mijn proefschrift is gericht aan een leken lezerspubliek en voor iedereen die ik niet wil lastig vallen met alle details, maar die toch graag zou willen weten over de essentie van het werk dat ik gedaan heb tijdens mijn promotie. Ik hoop dat ik met dit korte stukje in staat ben om enig inzicht te geven in de wereld van de biofysica en in de soms bizarre concepten van het fundamenteel onderzoek.
Tijdens mijn onderzoek heb ik mezelf voornamelijk bezig gehouden met biomembranen. Dergelijke membranen zijn een fundamenteel onderdeel van elke cel in ons lichaam en zijn essentieel voor het leven. Hun belangrijkste taak is de structurele organisatie van de cel, deze te scheiden van zijn omgeving en daarmee te definiëren als een eenheid. Bovendien organiseren zij de cel in kleinere compartimenten die verschillende functies vervullen. Membranen zijn ondoordringbaar voor de meeste in water oplosbare moleculen en daardoor zorgen zij ervoor dat elk molecuul op de juiste plek in de cel blijft waar het zijn functie vervult. Men kan membranen dus voorstellen als poortwachters die wat orde brengen in de chaos van cellulaire moleculen. Doordat de membranen een barrière vormen voor in water oplosbare moleculen creëren zij concentratiegradiënten van deze moleculen. Een dergelijke concentratiegradiënt is de drijvende kracht voor talloze biochemische processen, variërend van energieproductie tot signaaltransductie in neuronen. Vandaar dat biomembranen van groot belang zijn voor het functioneren van cellen.
Om beter te kunnen begrijpen hoe membranen functioneren moeten we inzoomen naar het moleculair niveau. En aangezien membranen gemiddeld slechts ongeveer vier nanometer (dat wil zeggen vier miljoenste van een millimeter) dik zijn, moet men nogal een beetje ver inzoomen. Van dichtbij zijn biomembranen complexe dynamische structuren waarvan de belangrijkste componenten kunnen worden onderverdeeld in twee klassen van moleculen: lipiden en eiwitten.
Lipiden zijn relatief kleine moleculen, bestaande uit een hydrofiele (water-minnende) kopgroep en hydrofobe (waterafstotende of vet-minnende) vetzuurketens. Omdat deze hydrofobe vetzuurketens zeer slecht oplosbaar zijn in water—denk aan oliedruppels in water—vormen lipiden dus spontaan een dubbele laag in waterige oplossingen (zie figuur). In dergelijke dubbellaagse membranen worden de vetzuurketens gericht naar de binnenzijde waar zij worden afgeschermd van de waterige omgeving, terwijl de kopgroepen contact maken met het water. Deze lipide dubbellaag vormt de basis van een biologische membraan en is verantwoordelijk voor de ondoordringbaarheid voor wateroplosbare stoffen.
De tweede component van biomembranen zijn de membraaneiwitten. Dit zijn moleculen die bestaan uit ketens van aminozuren en ze zijn over het algemeen veel groter dan lipiden. Het grote aantal mogelijke combinaties van aminozuren resulteert in een enorme verscheidenheid aan (membraan-) eiwitten met verschillende vormen en eigenschappen die verantwoordelijk zijn voor diverse taken. Sommige van deze membraaneiwitten versnellen biochemische reacties, bijvoorbeeld in de ademhalingsketen of tijdens de fotosynthese, processen die vooral plaatsvinden in membranen. Andere eiwitten zorgen dat de structuur van een cel of weefsel wordt gehandhaafd. Membraaneiwitten zijn ook verantwoordelijk voor selectieve transportprocessen van moleculen door de membraan en ze vormen een belangrijke schakel in de communicatie tussen verschillende cellen. Een voorbeeld hiervan zijn receptoren die boodschappermoleculen kunnen herkennen of betrokken zijn bij het activeren van cellen van het immuunsysteem. Deze complexiteit aan functies draagt bij tot het grote belang van membraaneiwitten in medisch onderzoek, iets wat goed geïllustreerd wordt door het feit dat ongeveer de helft van alle momenteel beschikbare geneesmiddelen werken op membraaneiwitten.
Opbouw van Biomembranen
membraaneiwitten
„lipid raft“
lipide dubbellaag
hydrofiel
fosfolipiden hydrofoob
cholesterol
hydrofiel
O
OH Structuur van SMA
–O O –O HO hydrofiel
O O hydrofoob
HO O– –O O
O O
HO O
styreeneenheid maleïnezuureenheid
Als men een individueel membraaneiwit beter wil bestuderen om meer inzicht te verkrijgen in hun functie loopt men snel tegen een vrij groot probleem aan. Het is belangrijk te beseffen dat membraaneiwitten afhankelijk zijn van hun natuurlijke omgeving om goed te functioneren, dat wil zeggen, van het samenleven met lipiden. Idealiter zou men dus graag eiwitten bestuderen in een levende cel. Er zijn echter weinig analysemethoden beschikbaar die daar gevoelig genoeg voor zijn. Dus om een bepaald eiwit te kunnen bestuderen is het nodig het eiwit te isoleren uit de cel en deze te scheiden van alle andere moleculen. Voor in water oplosbare eiwitten, zoals het hemoglobine in onze rode bloedcellen, is dit relatief eenvoudig. Membraaneiwitten zijn echter stevig verankerd in de membraan door hun hydrofobe oppervlakken. Hoewel dit noodzakelijk is voor hun functioneren, impliceert dit dat de membraan moet worden afgebroken om de verschillende membraaneiwitten te scheiden. De standaardmethode voor het afbreken van deze membranen is deze te solubiliseren (oplossen) met behulp van detergenten. In het dagelijks leven zijn deze aanwezig in zeep en ze worden gebruikt om vuil en vet op te lossen. Op soortgelijke manier, lossen de in het laboratorium gebruikte detergenten membraancomponenten op in water om hun scheiding mogelijk te maken. Een nadeel van deze methode is dat tijdens dit proces het eiwit vaak gedestabiliseerd raakt, waarbij er een risico is op inactivatie en aggregatie. Eiwitaggregatie is vergelijkbaar met de processen die plaatsvinden tijdens het stollen van een kippenei tijdens het koken, en in een dergelijke toestand geven eiwitten natuurlijk erg weinig informatie over hun functioneren in de cel. Het onderzoek naar membraaneiwitten is dus aanzienlijk problematischer dan onderzoek naar oplosbare eiwitten en de karakterisering van een enkel membraaneiwit overschrijdt dan ook veruit de gemiddelde duur van een promotietraject. Het gevolg daarvan is dat ons begrip van de functie van vele membraaneiwitten nog niet heel goed is.
Hiermee, na “slechts” twee pagina’s, ben ik aangekomen op het punt waar mijn onderzoeksproject begint. Maar geloof me, dit is waar het eigenlijk pas interessant wordt! Mijn project gaat over het ontwikkelen van een methode om membraaneiwitten efficiënt te verwijderen uit de membraan en daarbij hun natuurlijke omgeving te conserveren en ze te beschermen tegen aggregatie. Om dat te doen maken we gebruik van een amfifiel copolymeer bestaande uit styreen en maleïnezuur, (Engels: styrene maleic acid, kort SMA, zie figuur). Deze polymeer werd oorspronkelijk gebruikt als additief in de chemische industrie. Echter, SMA is ook onderzocht als een mogelijk transportsysteem voor het toedienen van medicijnen. In deze context hebben Britse wetenschappers min of meer bij toeval ontdekt dat SMA ook efficiënt werkt voor het oplossen van biomembranen. Het bijzondere is dat SMA de membraan niet volledig oplost zoals detergentia doen, maar het snijdt intacte ronde fragmenten uit de membraan, vergelijkbaar met een “cookie cutter”. Deze membraan schijven hebben een diameter van ongeveer tien nanometer en worden daarom aangeduid als nanodiscs (van nanometer en disc, het Engelse woord voor schijf). In 2009 werd al aangetoond dat membraaneiwitten kunnen worden toegevoegd aan zulke nanodiscs die dan vervolgens een stabiele omgeving voor het eiwit vormen.
Op het moment dat ik mijn onderzoek startte, werd deze methode pas door zeer weinig wetenschappers gebruikt en was het nog niet duidelijk in welke mate de SMA verenigbaar is met bestaande methoden in het onderzoek aan membraaneiwitten. Daarom hebben we ons gericht op het karakteriseren van SMA-nanodiscs om de mogelijkheden te kunnen beoordelen voor de studie van membraaneiwitten. De inzichten die we gaandeweg hebben opgedaan zijn beschreven in de lange versie van mijn proefschrift en zijn hieronder samengevat.
Hoofdstuk I is een algemene inleiding met een gedetailleerde beschrijving van biomembranen en hoe ze zijn opgebouwd. Daarna worden verschillende werkwijzen besproken die de solubilisatie van membraaneiwitten voor vervolgonderzoek mogelijk maken. De focus ligt hier op SMA-copolymeren en de toepassing daarvan als oplosmiddel voor membranen, wat het belangrijkste onderwerp van mijn proefschrift is.
Hoofdstuk II beschrijft een eerste onderzoeksproject waarin werd onderzocht hoe goed het polymeer werkt voor het oplossen en de zuivering van een membraaneiwit direct uit een biologische membraan. Als modeleiwit, kozen we een bacterieel kalium-ionkanaal dat structureel zeer vergelijkbaar is met veel humane kaliumkanalen. Op basis van dit modeleiwit konden we aantonen dat de solubilisatie met behulp van SMA een goed alternatief is voor gevestigde detergentmethoden waarmee gemakkelijke zuivering van het eiwit mogelijk is. Bovendien werd er vastgesteld dat het kaliumkanaal stabieler is in de SMA-nanodiscs dan in detergentia, wat een groot voordeel bleek tijdens latere experimenten. Daarnaast gebruikten we het gegeven dat de directe lipide omgeving van het kanaal werd meegezuiverd in de nanodiscs om zijn moleculaire samenstelling te onderzoeken. We hebben dus nu een nieuwe analytische methode die ons informatie kan geven over de voorkeur van het membraaneiwit voor zijn lipiden partners. Een nanodisc kan dus worden gezien als een momentopname van een eiwit in zijn natuurlijke membraanomgeving. Ten slotte zijn we erin geslaagd om het kanaal te transformeren in een kunstmatige lipide membraan, waarbij bleek dat de functionaliteit van het eiwit niet was aangetast door de isolatiemethode. Bovendien was dit experiment het eerste voorbeeld van de overdracht van een membraaneiwit in een kunstmatige membraan zonder dat het ooit in contact is geweest met potentiële schadelijke detergentia. Dit laatste in het bijzonder heeft een groot potentieel voor het onderzoek naar andere membraaneiwitten, vooral als deze erg gevoelig zijn voor detergentia.
In een verdere studie, beschreven in Hoofdstuk III, hebben we gekeken naar hoe verschillende lipide samenstellingen van de membraan van invloed zijn op de oplosbaarheid door SMA. Hiervoor gebruikten we modelmembranen zonder eiwitten om na te gaan of er een voorkeur was in het oplossen van verschillende lipiden door SMA. Informatie over een dergelijke voorkeur is belangrijk omdat dit potentieel van invloed kan zijn op conclusies over de geprefereerde lipide partners van membraaneiwitten (zie Hoofdstuk II). Door het systematisch variëren van de lipide samenstelling van modelmembranen, waren we in staat om aan te tonen dat er geen voorkeursbehandeling is van SMA tijdens het oplossen van membranen in een vloeibare toestand waarin de vetzuurketens van de lipiden relatief mobiel zijn. Dergelijke membranen worden zeer efficiënt opgelost door SMA en omgezet naar nanodiscs. Membranen in een geltoestand, met rigide opeengepakte vetzuurketens, worden echter zeer inefficiënt opgelost. De efficiëntie van het oplossen is dus sterk afhankelijk van de toestand waarin de membraanlipiden zijn. Een gevolg hiervan is dat er wel een voorkeur in de oplosbaarheid van membranen wordt waargenomen als deze zogenaamde fasescheiding vertonen. Membranen die fasescheiding vertonen bevatten tegelijkertijd domeinen (gebieden) in de vloeibare toestand en domeinen in de geltoestand, en beide domeinen verschillen in lipide samenstelling. In deze situatie worden de vloeibare domeinen veel sneller opgelost door SMA.
Dergelijke voorkeur in de oplosbaarheid van vloeibare domeinen zou mogelijk een toepassing kunnen hebben voor het bestuderen zogenaamde “lipid rafts” (letterlijk lipide vlotten). Dergelijke rafts zijn sterk geordende membraandomeinen die mogelijk aanwezig zijn in de membraan van levende cellen, bijvoorbeeld in het immuunsysteem, en er wordt aangenomen dat deze domeinen een specifieke functie vervullen. Echter, in de afgelopen twintig jaar is er een zeer controversieel debat gaande onder membraanonderzoekers over het belang van lipid rafts. En inderdaad is tot op de dag van vandaag het bestaan van deze rafts noch bevestigd noch ontkracht en wordt er nog steeds actief onderzoek gedaan op dit gebied.
Hoofdstuk IV beschrijft een studie waarin het effect van SMA op menselijke kankercellen onderzocht wordt om verdere informatie te verkrijgen over de oplosbaarheid. Met behulp van een speciale microscopietechniek konden we video’s maken waardoor we live konden volgen hoe levende cellen worden opgelost door de SMA. Hiervoor werden de celkweken gesupplementeerd met kunstmatig DNA, dat vervolgens door de cellen werd opgenomen en gebruikt als bouwplan voor het maken van verschillende eiwitten. Deze bouwplannen zijn zodanig ontworpen dat de eiwitten fluorescent zijn. Dit betekent dat wanneer de cellen worden blootgesteld aan licht met een specifieke golflengte, dat wil zeggen licht met een specifieke kleur, ze licht uitstralen met een hogere golflengte, dat wil zeggen, een andere kleur. Het fluorescente licht kan vervolgens worden gedetecteerd met een speciale microscoop waardoor de visualisatie van individuele cellulaire compartimenten mogelijk is. Met deze methode we onderzocht of er verschillen zijn in de snelheid waarmee de membranen van de verschillende cellulaire compartimenten worden opgelost door SMA. Het was verrassend dat we aantoonden dat de plasmamembraan (de buitenlaag van de cel) het langzaamst oplost, ook al is deze laag de eerste die in contact komt met SMA. Verder zagen we dat verschillende eiwitten in het plasmamembraan met verschillende snelheden werden opgelost. Ook deze resultaten suggereren dat lipid rafts mogelijk invloed hebben op het oplossen van de membraan (zie Hoofdstuk III).
Voor het onderzoek beschreven in Hoofdstuk V, keerden we terug naar de hierboven genoemde bacteriële membranen met het kaliumkanaal (zie Hoofdstuk II). We gebruikten deze als modelsysteem om de experimentele condities voor de solubilisatie van membraaneiwitten door SMA te optimaliseren. Met deze aanpak konden wij aantonen dat verschillende factoren bestaan die in verschillende mate invloed hebben op de efficiëntie van de solubilisatie, en hebben we condities geoptimaliseerd die de solubilisatie van eiwitten bevorderen. We vonden dat de invloed van de zoutconcentratie en pH bijzonder groot is. Zeer lage of zeer hoge zoutconcentraties voorkomen het oplossen van de membraan bijna volledig, dit kan vooral worden verklaard door de eigenschappen van de SMA polymeer zelf. Alleen zoutconcentraties die lijken op de fysiologische zoutconcentratie in ons lichaam bevorderen het oplosbaar vermogen van de SMA, zie figuur. Voor de pH vonden we het omgekeerde effect voor de bacteriële membranen vergeleken met wat eerder is waargenomen voor modelmembranen zonder eiwit. Dit lijkt paradoxaal, maar er zijn hiervoor verschillende mogelijke verklaringen aan te dragen. De meest waarschijnlijke daarvan is dat de pH-afhankelijkheid van de membraanoplosbaarheid sterk gerelateerd is aan de lipide samenstelling van de membraan. Er zijn echter nog verdere studies nodig om hier een duidelijker beeld van te krijgen. Dit voorbeeld toont dan ook heel mooi aan dat er nog veel werk gedaan moet worden om volledig te begrijpen hoe het oplossen van een membraan met behulp van SMA werkt. Echter, een beter begrip van dit proces is noodzakelijk om het volledige potentieel van deze methode te kunnen begrijpen.
In Hoofdstuk VI worden onze resultaten in de context geplaatst van wetenschappelijke studies van andere auteurs in het kader van een algemene discussie. Verder wordt er een vooruitzicht gegeven op toepassingen van solubilisatie van membranen door SMA en worden eventuele beperkingen van de methode besproken. Als conclusie kan worden gegeven dat de studies die tot nu toe uitgevoerd zijn met SMA veelbelovende resultaten laten zien die veelzijdige toepassingen in het membraanonderzoek kunnen hebben. Het is daarom zeer waarschijnlijk dat SMA-polymeren een grote bijdrage gaan leveren aan een beter begrip van biomembranen.
Tot slot wil ik graag kort (dit keer echt) proberen om een veel gestelde vraag te beantwoorden: “En waar is dit goed voor?”. Allereerst is dit een hele goede vraag. Helaas is het antwoord niet heel eenvoudig en een volledig antwoord valt echt buiten de strekking van dit proefschrift. Het kortste antwoord dat ik kan bedenken is: “Alles en niets”. Alles, omdat de kennis die we hebben gegenereerd kan worden gebruikt in een groot aantal toepassingen. En niets omdat we zelf niet echt als doelstelling hebben om deze applicaties zelf te ontwikkelen en dit is ook niet de focus van ons werk. Ons onderzoek heeft als algemene doelstelling het verkrijgen van een beter begrip over biomembranen en membraaneiwitten, en daarvoor hebben we de mogelijkheden van een nieuwe methode onderzocht. Dit soort op kennis gefocuste wetenschap heet daarom fundamenteel onderzoek. Volgens de uitdrukking “kennis is macht”, kunnen inzichten die worden verkregen op deze manier dan vervolgens dienen als de basis voor verder toegepast onderzoek. Als fundamentele onderzoekers zijn we dus minder bezig met een specifieke toepassing, bijvoorbeeld om een remedie voor een specifieke ziekte te ontwikkelen. Men kan echter stellen dat de resultaten verkregen met ons onderzoek kunnen helpen om nieuwe remedies voor allerlei ziekten te vinden. Dit omdat ziekten vaak op een één of andere manier geassocieerd zijn met membraanprocessen en inzicht in hun fundamentele principes is cruciaal voor de ontwikkeling van geneesmiddelen. In dit verband wil ik er ook graag op wijzen dat vele baanbrekende wetenschappelijke prestaties mogelijk zijn gemaakt door fundamenteel onderzoek. Bijvoorbeeld, de ontdekking van het allereerste antibioticum, penicilline, was een nogal gelukkig toeval (een schimmel had een petrischaal met bacteriën geïnfecteerd en bleek ze te doden). En het is alleen te danken aan de nieuwsgierigheid van de wetenschapper die deze waarneming maakte dat de basis werd gelegd voor de ontwikkeling van antibiotica. De SMA-copolymeer is ook slechts bij toeval ontdekt voor zijn toepassing op het gebied van het membraanonderzoek. Het is echter zeer moeilijk om nu al in te schatten wat er over tien of vijftig jaar geworden zal zijn van ons SMA-onderzoek naar membraaneiwitten. Het zal waarschijnlijk niet leiden tot een revolutie in de geneeskunde vergelijkbaar met penicilline, en wellicht is het uiteindelijk totaal vergeten. Maar misschien zal ons onderzoek een bijdrage leveren aan een andere doorbraak, wie weet? Enkel één ding is zeker: het is de moeite waard!
Bekijk ook deze proefschriften
Structure-Preserving Data-Driven Methods for Modeling Turbulent Flows
Molecular insights into the role of VRS5 in tillering and lateral spikelet development in barley
Gamma Knife Radiosurgery for Skull Base Tumors
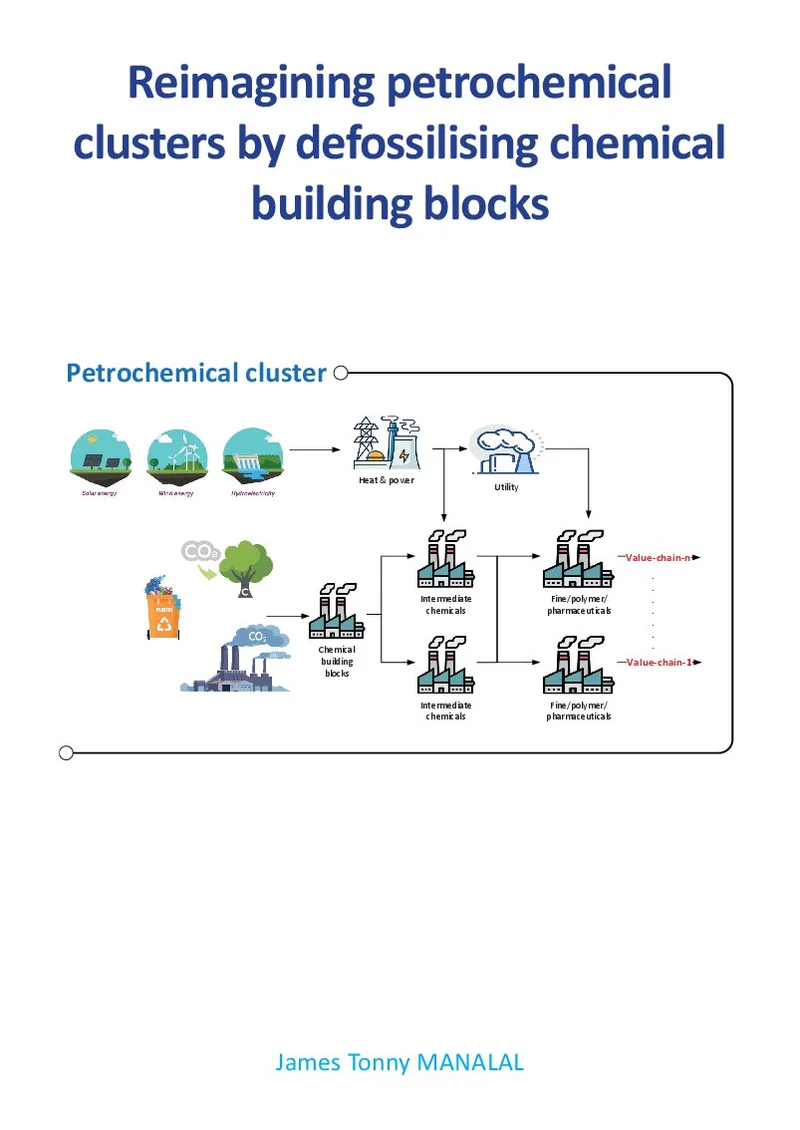
Reimagining petrochemical clusters by defossilising chemical building blocks
Microbial stabilization and protein functionality of plant-based liquids using pulsed electric fields
Wij drukken voor de volgende universiteiten