Deel dit project
Treatment optimisation and pharmacogenetics of systemic and intraperitoneal chemotherapy in colorectal cancer
Samenvatting
De behandeling van patiënten met colorectale kanker bestaat vaak uit chemotherapie. De behandeling met deze chemotherapie is echter niet zonder bijwerkingen. Deze bijwerkingen kunnen leiden tot een verminderde kwaliteit van leven, het vroegtijdig stopzetten van een behandeling en soms zelfs tot overlijden. Bovendien is de kans op genezing bij patiënten met uitgezaaide kanker klein. Er valt dus nog veel te verbeteren aan de behandeling van colorectale kanker, zowel op het gebied van veiligheid als werkzaamheid. Een oplossingsrichting om deze behandeling te verbeteren voor de individuele patiënt, zou het gebruik van nieuwe genetische biomarkers kunnen zijn. Het gebruik van deze biomarkers maakt het mogelijk om patiënten te identificeren die een hoger risico hebben op ernstige geneesmiddelgerelateerde bijwerkingen, en om patiënten te selecteren die het meest zullen profiteren van chemotherapie. Het doel van dit proefschrift was derhalve de verbetering van de veiligheid en werkzaamheid van chemotherapie bij patiënten met colorectale kanker door middel van de identificatie en validatie van genetische biomarkers die gepersonaliseerde dosering mogelijk maken en mogelijk voorspellend zijn voor behandeluitkomsten.
In Deel I van dit proefschrift hebben we ons gericht op het optimaliseren van de systemische behandeling met irinotecan. Ons doel was om de toegevoegde waarde en de klinische bruikbaarheid van het gepersonaliseerd doseren van irinotecan op basis van UGT1A1 genotype te onderzoeken. Dit hebben we gedaan door middel van een systematische literatuurreview and de ontwikkeling van een richtlijn over de geneesmiddel-gen interactie tussen irinotecan and UGT1A1. Voor het ultieme bewijs hebben we een prospectieve implementatiestudie uitgevoerd waarbij we het gepersonaliseerd doseren van irinotecan op basis van UGT1A1 genotype in de klinische setting hebben getoetst.
In Hoofdstuk 2 hebben we de potentiële waarde van het gepersonaliseerd doseren van irinotecan op basis van UGT1A1 genotype getoetst aan de hand van de beschikbare literatuur. Er is hierbij geëvalueerd of het gepersonaliseerd doseren van irinotecan het risico op ernstige toxiciteit vermindert. Dit is uitgevoerd op basis van vijf vooraf gespecificeerde criteria: 1] het niveau van bewijs voor de associatie tussen UGT1A1 polymorfismen en door irinotecan-geïnduceerde ernstige toxiciteit, 2] de klinische validiteit en bruikbaarheid van UGT1A1 genotypering voorafgaand aan start irinotecan, 3] de veiligheid en tolerantie van irinotecan bij dragers van UGT1A1 polymorfismen, 4] de beschikbaarheid van doseringsaanbevelingen voor irinotecan bij dragers van UGT1A1 polymorfismen, en 5] de financiële voordelen van gepersonaliseerd doseren van irinotecan. Alle vijf criteria gaven aan dat gepersonaliseerd doseren van irinotecan van waarde is. Het hoogste niveau van bewijs (niveau I) werd gevonden voor een hogere incidentie van irinotecan-geïnduceerde ernstige toxiciteit bij homozygote dragers van UGT1A1*28 of UGT1A1*6 (UGT1A1 PMs); de klinische validiteit en bruikbaarheid van de UGT1A1 genotypering bleken acceptabel te zijn; in dose-finding studies werd een lagere maximaal getolereerde dosis gezien bij UGT1A1 PMs; en de meeste drug labels en richtlijnen bevelen een dosisvermindering van 25 tot 30% aan UGT1A1 PMs. Bovendien is het gepersonaliseerd doseren van irinotecan waarschijnlijk kosteneffectief.
Hoofdstuk 3 had als doel om een richtlijn voor artsen en apothekers te ontwikkelen over het gepersonaliseerd doseren van irinotecan op basis van UGT1A1 genotype. Deze richtlijn is geschreven namens de Nederlandse Farmacogenetica Werkgroep (DPWG) en met deze richtlijn wordt beoogd de implementatie van deze genotypering in de klinische praktijk te vergemakkelijken. De richtlijn is gebaseerd op een systematische literatuurreview. Zoals ook gerapporteerd in Hoofdstuk 2 is er voor UGT1A1 PMs voldoende bewijs dat er sprake is van een verhoogd risico op ernstige bijwerkingen zoals neutropenie of diarree bij normale doses (ook in vergelijking met alle andere genotypen/fenotypen), terwijl overtuigend bewijs voor verhoogde werkzaamheid niet is aangetoond. Dit verhoogde risico op toxiciteit werd gerapporteerd in alle negen geïncludeerde meta-analyses en in 16 van de 23 geïncludeerde studies. Met betrekking tot de werkzaamheid bleek uit vier van de vijf meta-analyses en acht van de tien studies dat er geen verband bestond tussen de *28 en/of *6 varianten en een verhoogde effectiviteit van de behandeling. Op basis van farmacokinetische studies beveelt deze DPWG-richtlijn een startdosis van 70% aan bij UGT1A1 PM patiënten die starten met irinotecan. Bij UGT1A1 intermediaire metaboliser patiënten wordt geen dosisverlaging bij start irinotecan aanbevolen. Op basis van de DPWG clinical implication score wordt UGT1A1 genotypering als “essentieel” beschouwd, hiermee geeft de DPWG aan dat UGT1A1 genotypering standaard uitgevoerd zou moeten worden voorafgaand aan behandeling met irinotecan.
In Hoofdstuk 4 wordt een prospectieve implementatiestudie beschreven naar het gepersonaliseerd doseren van irinotecan op basis van UGT1A1 genotype. Dit is naar ons weten de eerste prospectieve implementatiestudie waarbij irinotecan wordt gedoseerd op basis van UGT1A1. Uit deze studie blijkt dat het gepersonaliseerd doseren leidt tot een significante verlaging van de incidentie van febriele neutropenie en het aantal door chemotherapie-geïnduceerde ziekenhuisopnames bij UGT1A1 PMs. Van de 350 geïncludeerde patiënten waren 31 (8,9%) patiënten UGT1A1 PM. Deze groep patiënten is behandeld met een mediane dosisintensiteit irinotecan van 70%. De incidentie van febriele neutropenie in deze groep was 6,5% in vergelijking met 24% bij historische UGT1A1 PMs die met een 100% dosering behandeld werden (p=0,04). De incidentie van 6,5% in UGT1A1 PMs was vergelijkbaar met de incidentie bij UGT1A1 non-PMs behandeld met de volledige dosis irinotecan. De systemische blootstelling van SN-38 bij UGT1A1 PMs, die behandeld werden met een 70% dosisintensiteit, was nog steeds licht hoger in vergelijking met een patiëntencohort behandeld met een standaard 100% dosisintensiteit van irinotecan (verschil: +32%). De kostenanalyse toonde aan dat gepersonaliseerd doseren van irinotecan kostenbesparend was, de kosten werden verlaagd met €183 per patiënt. Met dit hoofdstuk is aangetoond dat het gepersonaliseerd doseren van irinotecan op basis van UGT1A1 genotype de patiëntveiligheid significant verbetert zonder risico op onderdosering. Hiermee is het gepersonaliseerd doseren van irinotecan succesvol geïmplementeerd in vier Nederlandse ziekenhuizen en we bevelen dan ook landelijke implementatie aan.
In Deel II lag de focus op de optimalisatie van intraperitoneale chemotherapie bij patiënten met colorectale peritoneale metastasen. Het doel was om genetische biomarkers te identificeren die voorspellend zijn voor de behandeluitkomsten van cytoreductieve chirurgie plus hypertherme intraperitoneale chemotherapie (CRS + HIPEC).
Om dit te bereiken hebben we in Hoofdstuk 5 eerst een systematische literatuurreview uitgevoerd naar de associatie tussen genetische biomarkers in de DNA repair pathway en behandeluitkomsten van patiënten die behandeld werden met CRS + HIPEC. Hierbij is gekeken naar patiënten die behandeld werden met mitomycine of oxaliplatine. Aangezien de literatuur over intraperitoneale chemotherapie en genetische biomarkers schaars was, is de zoekstrategie uitgebreid naar systemische chemotherapie. In totaal werden 43 artikelen opgenomen in deze review. Geen enkele studie meldde potentiële farmacogenetische biomarkers bij patiënten met colorectale kanker die mitomycine-gebaseerde systemische chemotherapie ondergingen. Voor oxaliplatine-gebaseerde systemische chemotherapie werden in totaal 26 genetische biomarkers binnen 14 genen geïdentificeerd die significant geassocieerd waren met de behandeluitkomsten. De meest veelbelovende genetische biomarkers waren ERCC1 rs11615, XPC rs1043953, XPD rs13181, XPG rs17655, MNAT rs3783819/rs973063/rs4151330, MMR-status, ATM-eiwitexpressie, HIC1 tandem repeat DN7SS en PIN1 rs2233678. Deze resultaten voor de behandeluitkomsten van systemisch oxaliplatine kunnen mogelijk geëxtrapoleerd worden naar intraperitoneale oxaliplatine. Dit systematische review biedt de basis voor dit verdere onderzoek.
In Hoofdstuk 6 hebben we een retrospectieve genoomwijde associatiestudie (GWAS) uitgevoerd in een colorectale kankerpatiëntencohort van 258 patiënten. Deze patiënten werden behandeld met CRS + HIPEC met oxaliplatine en mitomycine. Met deze GWAS wilden we nieuwe genetische biomarkers identificeren die mogelijk geassocieerd zijn met de behandeluitkomsten van CRS + HIPEC. De studie toonde twaalf markers aan die significant geassocieerd waren met ziektevrije overleving en die de expressie van zes genen beïnvloeden. Voor vier van deze zes geïdentificeerde genen (FAMPB, STAGN, SCLPSG2 en METTL22) konden één of meer biologische mechanismen worden geïdentificeerd die de waargenomen associaties tussen de genetische biomarkers met verminderde ziektevrije overleving ondersteunen. Verschillende nieuwe potentiële prognostische of predictieve genetische biomarkers voor de klinische uitkomst van CRS + HIPEC patiënten werden geïdentificeerd. Dit is de eerste GWAS-studie in deze type patiëntenpopulatie, en voordat deze bevindingen klinisch kunnen worden toegepast, is verdere validatie van de gegevens in een onafhankelijk patiëntencohort nodig.
Hoofdstuk 7 omvat een retrospectieve studie waarbij NQO1*2, NQO1*3 en POR*28 als mogelijke genetische biomarkers voor HIPEC met mitomycine klinisch werden gevalideerd. Mitomycine is een prodrug die wordt geactiveerd door de enzymen NQO1 en POR. Echter, niet alle patiënten zijn in staat om mitomycine te activeren, bijvoorbeeld als gevolg van polymorfismen in de genen die voor deze enzymen coderen. Het doel van deze studie was om de associatie tussen NQO1*2, NQO1*3 en POR*28 en de behandeluitkomsten van CRS + HIPEC met mitomycine te onderzoeken. Dit werd uitgevoerd bij patiënten die peritoneale metastasen hadden van colorectale kanker. In deze retrospectieve studie werden in totaal 253 patiënten geïncludeerd. Hierbij werd een significante associatie gevonden tussen dragers van NQO1*3 en een hogere peritoneal recurrence rate. De peritoneal recurrence rate 3 en 6 maanden na HIPEC was significant hoger dan bij wildtype patiënten, respectievelijk 30,0% versus 3,8% (p=0,009) en 40,0% versus 12,1% (p=0,031). In lijn met deze resultaten werd dragerschap van NQO1*3 geassocieerd met een kortere ziektevrije overleving (HR 2,04, 95% BI [1,03–4,03]). Er was geen significante associatie met overall survival (HR 1,42, 95% BI [0,66–3,07]). Deze resultaten suggereren dat de individualisering van patiënten die behandeld worden met CRS + HIPEC op basis van farmacogenetica gunstig kan zijn en dat dit verder onderzocht zou moeten worden.
Dit proefschrift heeft ons een paar stappen dichterbij veilig en effectief gebruik van chemotherapie voor de individuele colorectale kankerpatiënt gebracht. Irinotecan zou niet meer moeten worden gestart zonder een UGT1A1 genotypering vooraf en een eerste stap is gemaakt richting het gepersonaliseerd doseren van intraperitoneale chemotherapie bij colorectale kankerpatiënten met peritoneale metastasen.
Bekijk ook deze proefschriften
Structure-Preserving Data-Driven Methods for Modeling Turbulent Flows
Molecular insights into the role of VRS5 in tillering and lateral spikelet development in barley
Gamma Knife Radiosurgery for Skull Base Tumors
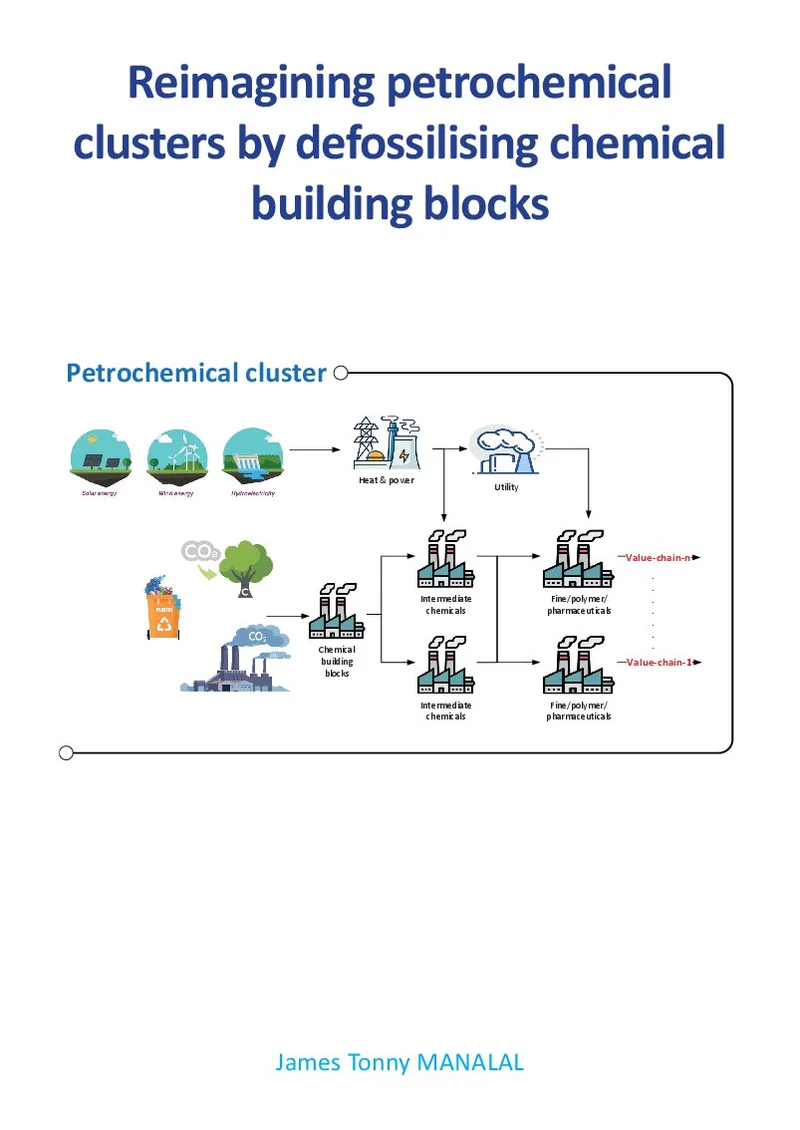
Reimagining petrochemical clusters by defossilising chemical building blocks
Microbial stabilization and protein functionality of plant-based liquids using pulsed electric fields
Wij drukken voor de volgende universiteiten