Deel dit project
Towards a better future for children with SLE
Samenvatting
Systemische lupus erythematosus (SLE) is een ernstige en potentieel levensbedreigende auto-immuunziekte. SLE die op de kinderleeftijd begint (cSLE) vertoont doorgaans een ernstiger klinisch verloop dan SLE bij volwassenen. Dit heeft aanzienlijke gevolgen voor de kwaliteit van leven, onderwijsprestaties en participatie op de arbeidsmarkt van deze patiënten. Meer dan de helft van de patiënten slaagt er niet in om op jongvolwassen leeftijd betaald werk te vinden. Tegen de tijd dat patiënten de leeftijd van 30 jaar bereiken, zal 5-10% van hen zijn overleden als direct gevolg van SLE en voornamelijk door infecties of cardiovasculaire complicaties. Op die leeftijd heeft de meerderheid van de overlevende patiënten inmiddels ook onomkeerbare schade opgelopen door zowel de ziekte zelf als door de medicamenteuze behandeling ervan. Met name prednison geeft een aanzienlijk verhoogd risico op het ontwikkelen van schade zoals onder andere cataract, osteoporose, osteonecrose, groeivertraging of zelfs groeistilstand. Het is daarom van groot belang om behandelingen te ontwikkelen die de ziekteactiviteit kunnen verminderen terwijl de schadelijke effecten van zowel de ziekte als de medicatie worden geminimaliseerd.
Er zijn drie potentiele strategieën die kunnen bijdragen aan de verbetering van de behandeling. Een recent ontwikkelde therapeutische strategie is het zogenaamde “treat-to-target” (T2T) concept. Hierin wordt de behandeling aangepast op geleide van de ziekteactiviteit om een vooraf bepaald doel (remissie of lage ziekteactiviteit) te bereiken. Hoewel dit concept reeds is uitgewerkt voor SLE bij volwassenen, is de haalbaarheid ervan bij kinderen met SLE tot op heden niet onderzocht. Ten tweede kunnen therapeutische interventies worden geoptimaliseerd door het identificeren van meetbare biomarkers, die bijdragen aan de pathogenese en daardoor geassocieerd zijn met ziekteactiviteit. Type I Interferonen (IFN-I) zijn een groep eiwitten die een belangrijke rol spelen in de pathogenese van SLE. Daarom vormen deze eiwitten een veelbelovende biomarker voor ziekteactiviteit. Met de komst van medicijnen die de IFN-I route kunnen blokkeren kan de aanwezigheid van deze eiwitten gebruikt worden om patiënten te selecteren die gebaat zouden kunnen zijn bij deze nieuwe behandelmethodes. Naast de IFN-I route zijn in recente studies andere eiwit en/of gen profielen geassocieerd met de mate van ziekteactiviteit in SLE. Daarom kan een derde strategie om de behandeling van SLE te optimaliseren, bestaan uit het combineren van de eiwit en gen-profielen die geassocieerd zijn met ziekteactiviteit. In dit proefschrift zullen we middels diverse studies laten zien dat deze strategieën een cruciale rol kunnen spelen bij het optimaliseren van de behandeling van kinderen met SLE.
In Hoofdstuk 1 beschrijven we de klinische kenmerken van cSLE, waarbij wordt benadrukt dat er momenteel geen diagnostische criteria bestaan voor deze ziekte en dat verschillende methoden worden gebruikt om de ziekteactiviteit te beoordelen. Bovendien bespreken we de gebruikte instrumenten om ziekteactiviteit, opvlammingen en ziekte gerelateerde schade te meten. Daarnaast behandelen we de nieuwste therapeutische doelen, met nadruk op de T2T-benadering die positieve resultaten heeft laten zien bij volwassenen met SLE. Wat betreft de pathogenese bespreken we de rol van verschillende triggers bij het ontstaan van de ziekte en hun bijdrage aan het in stand houden van de ziekte. Tevens leggen we uit hoe het aangeboren en verworven deel van het immuunsysteem met elkaar samenwerken en resulteren in de zogenaamde zelfversterkende immunologische cyclus die als kenmerk van de pathogenese van SLE wordt gezien. We sluiten dit hoofdstuk af door de belangrijke rol van IFN-I eiwitten te bespreken. Zoals reeds genoemd, wordt IFN-I gezien als een belangrijke speler in de pathogenese van SLE. Deze eiwitten kunnen niet alleen dienen als een veelbelovende kandidaat-biomarker voor het monitoren van ziekteactiviteit, maar worden in klinische trials ook gebruikt als een therapeutisch doelwit en geremd middels verschillende medicijnen.
De farmacologische behandeling van SLE-patiënten heeft als doel ziekteremissie te bereiken. Zowel klinische remissie als de recent geformuleerde staat van lage ziekte activiteit, “Low Lupus Disease Activity State” (LLDAS), zijn therapeutische doelen die geassocieerd worden met een lager risico op ziekteopvlammingen en orgaanschade. In Hoofdstuk 2 tonen we aan dat LLDAS een haalbaar behandelingsdoel is voor kinderen met SLE. In het Rotterdamse cohort behaalden alle kinderen LLDAS binnen een mediane tijd van 6 maanden. Tevens werd aangetoond dat het voorschrijven van immunosuppressiva in een vroeg stadium het gebruik van corticosteroïden kan beperken. Het streven naar LLDAS lijkt hiermee een haalbaar doel in cSLE en zal naar verwachting leiden tot betere lange termijn resultaten, waaronder verminderde orgaanschade en minder ziekteopvlammingen.
Hoewel de klinische kenmerken van SLE waardevolle inzichten geven in de ziekteactiviteit en het optreden van ziekteopvlammingen, is er behoefte aan specifieke parameters die de onderliggende afwijkende biologische routes beter weergeven. In Hoofdstuk 3.1 tonen we aan dat een subset van patiënten met cSLE een verhoogde expressie vertoont van IFN-I, de zogenaamde IFN-I handtekening. Opmerkelijk is dat bij deze patiënten de expressie van de endoplasmatische en cytoplasmatische receptoren, die verantwoordelijk kunnen zijn voor het aanzetten van IFN-I productie, verhoogd zijn ondanks het gebruik van verschillende medicijnen. We waren in staat om de IFN-I handtekening te remmen door het TBK-1 eiwit te blokkeren. Dit eiwit maakt deel uit van de IFN-I signaalroute. Daarom zou TBK-1 in de toekomst een nieuw therapeutisch aangrijpingspunt in SLE kunnen zijn.
Bijna alle patiënten met SLE die tot op heden werden geïncludeerd in verschillende wetenschappelijke studies waarin de IFN-I handtekening werd bepaald, hadden al een behandeling met één of meerdere medicijnen ondergaan. Interessant genoeg vertoonde echter de meerderheid van deze patiënten nog steeds een verhoogde IFN-I handtekening ondanks deze behandelingen. Om dit nader te onderzoeken, hebben we in Hoofdstuk 3.2 een in vitro model opgezet waarin we het effect van verschillende veelgebruikte medicijnen in SLE hebben getest in cellen waar de IFN-I productie werd aangezet door de endoplasmatische en/of cytoplasmatische routes te activeren. Aangezien de geteste medicatie geen effect leek te hebben op IFN-I aanmaak via de cytoplasmatische routes, verloopt de aanhoudende productie van IFN-I waarschijnlijk via deze receptoren.
Verschillende onderzoeken geven aan dat de IFN-I handtekening een potentiële biomarker voor ziekteactiviteit is. Meerdere longitudinale studies hebben echter tegenstrijdige resultaten opgeleverd. In Hoofdstuk 3.3 is een uitgebreide longitudinale cohortstudie beschreven. In deze studie hebben we zowel de IFN-I handtekening als de concentratie van IFN-I eiwitten bepaald. IFN-alpha2, één van de belangrijkste IFN-I eiwitten, werd gemeten met behulp van een zeer gevoelige Single-molecule assay genaamd Simoa. Met de Simoa techniek kunnen zeer lage concentraties van IFN-alpha2 worden gemeten. Onze resultaten toonden aan dat de IFN-I handtekening relatief stabiel bleef gedurende een periode van drie jaar en niet significant geassocieerd was met ziekteactiviteit. Echter zagen we dat de concentratie van IFN-alpha2 in het bloed, gemeten met Simoa, in de loop van de tijd schommelde en geassocieerd was met veranderingen in ziekteactiviteit. Dit laat zien dat de methode waarmee IFN-I activiteit wordt gemeten van essentieel belang is voor de toepasbaarheid in de kliniek als biomarker voor ziekteactiviteit.
De IFN-I handtekening is niet het enige genexpressieprofiel dat geassocieerd is met SLE. Eerdere onderzoeken hebben aangetoond dat er meerdere genexpressieprofielen geassocieerd zijn met cSLE. Een combinatie van deze profielen kan worden gebruikt om patiënten in meer homogene groepen te verdelen op basis van hun ziekteactiviteit. De technieken gebruikt in de gepubliceerde landmark studie zijn echter vaak te complex en kostbaar voor de dagelijkse klinische praktijk. In Hoofdstuk 4.1 hebben we deze gen-expressieprofielen vertaald naar vier eenvoudigere gen-handtekeningen die makkelijker toepasbaar zouden kunnen zijn in de klinische praktijk. Wij toonden aan dat een combinatie van deze handtekeningen in staat is om patiënten in te delen in groepen met vergelijkbare ziekteactiviteits-profielen. In een vervolgstudie, Hoofdstuk 4.2, werden deze gen-handtekeningen gecombineerd met specifieke eiwitten die eveneens geassocieerd zijn met SLE. Vervolgens werd een computermodel gebruikt om patiënten op basis van deze biologische factoren (genexpressie en eiwitten) in verschillende groepen in te delen. Deze benadering resulteerde in drie duidelijke clusters van patiënten met verschillende ziekteactiviteits-kenmerken. Bovendien onderzochten we via 40-kleuren flowcytometrie of de gevonden clusters gekarakteriseerd werden door specifieke celtypen in perifeer bloed. Intrigerend genoeg werden meerdere celtypen gevonden die verschilden tussen deze clusters. Gezamenlijk benadrukken deze twee studies het idee dat toekomstige behandelingsbeslissingen niet alleen gebaseerd moeten zijn op klinische kenmerken, maar ook nieuwe biologische parameters moeten omvatten.
In Hoofdstuk 5 vergelijken we onze bevindingen met de bestaande literatuur. Meerdere recente studies hebben aangetoond dat het bereiken van LLDAS een haalbaar doel is in cSLE. Het is echter belangrijk op te merken dat de huidige definitie van LLDAS is afgestemd op volwassenen. Dankzij de inspanningen van een internationale taskforce zijn er nu definities voor kinderen vastgesteld die sterk lijken op die voor volwassenen, wat de vergelijkbaarheid van toekomstige studies tussen pediatrische en volwassen populaties vergemakkelijkt. Hoewel de resultaten overwegend positief zijn voor de T2T-benadering, bestaan er nog ideeën om deze strategie verder te verfijnen. Een van deze ideeën is het toevoegen van een meetbare biologische parameter aan de T2T-criteria. Deze biomarker dient het liefst geassocieerd te zijn met de ziekteactiviteit waardoor de T2T-doelstelling ook op biologisch gebied behaald kan worden. IFN-I lijkt veelbelovend in dit opzicht, maar er lijken zich op meerdere niveaus (genomics, transcriptomics, proteomics etc.) kandidaten te melden die voor dit doeleinde kunnen worden gebruikt. Met de komst van nieuwe analysemethodes, waaronder artificiële intelligentie lijkt onderzoek waarin kandidaten uit meerdere niveaus worden gecombineerd nog relevanter. De vraag blijft echter of deze benadering in de praktijk haalbaar is, rekening houdend met factoren zoals kosten en technische haalbaarheid. Daarom blijft het de verantwoordelijkheid van onderzoekers om technieken te ontwikkelen die zowel kosteneffectief als haalbaar zijn voor de klinische praktijk.
Systemic lupus erythematosus (SLE) is a severe and potentially life-threatening autoimmune disease. SLE that begins in childhood (cSLE) typically exhibits a more severe clinical course than SLE in adults. This has significant implications for the quality of life, educational achievements, and employment opportunities of these patients. More than half of the patients fail to secure paid employment in young adulthood. By the time patients reach the age of 30, 5-10% of them will have died as a direct result of SLE, mainly due to infections or cardiovascular complications. At that age, the majority of surviving patients have also incurred irreversible damage from both the disease itself as its pharmacological treatment. Specifically, prednisone poses a significantly increased risk of developing damage such as cataracts, osteoporosis, osteonecrosis, growth delay, or even growth cessation. Therefore, it is important to develop therapeutic strategies that can reduce disease activity while minimizing the detrimental effects of both the disease and medication.
There are three potential strategies that can contribute to improving treatment. A recently developed therapeutic strategy is the so-called “treat-to-target” (T2T) concept. Here, treatment is adjusted based on disease activity to achieve a predetermined goal (remission or low disease activity). Although this concept has already been elaborated for SLE in adults, its feasibility in children with SLE has not been explored to date. Second, therapeutic interventions can be optimized by identifying measurable biomarkers that contribute to pathogenesis and are therefore associated with disease activity. Type I Interferons (IFN-I) are a group of proteins that play an important role in the pathogenesis of SLE. Therefore, these proteins represent a promising biomarker for disease activity. With the advent of drugs that can block the IFN-I pathway, the presence of these proteins can be used to select patients who may benefit from these new drugs. In addition to the IFN-I pathway, recent studies have associated other protein and/or gene profiles with the degree of disease activity in SLE. Therefore, a third strategy to optimize the treatment of SLE may involve combining the protein and gene profiles associated with disease activity. In this thesis, through various studies, we will confirm that the aforementioned strategies can play a crucial role in optimizing the treatment of children with SLE.
In Chapter 1, we delineate the clinical characteristics of cSLE, emphasizing the absence of current diagnostic criteria for this condition and the utilization of various methods to assess disease activity. Additionally, we discuss the tools employed for measuring disease activity, flares, and disease-related damage. Furthermore, we address the latest therapeutic targets, with a focus on the T2T approach that has shown positive outcomes in adults with SLE. Regarding the pathogenesis, we discuss the role of various triggers in the onset of the disease and their contribution to its maintenance. We also discuss how the innate and adaptive part of the immune system collaborate and result in the so-called self-amplifying immunological loop, recognized as a hallmark of SLE pathogenesis. This chapter concludes by discussing the pivotal role of IFN-I. As previously mentioned, IFN-I is regarded as a key player in the pathogenesis of SLE. These proteins not only serve as promising candidate biomarkers for monitoring disease activity but are also employed as a therapeutic target in clinical trials, being inhibited by various medications.
The pharmacological treatment of SLE patients aims to achieve disease remission. Both clinical remission and the more recently formulated state of low disease activity, known as “Low Lupus Disease Activity State” (LLDAS), are therapeutic goals associated with a reduced risk of disease flares and organ damage. In Chapter 2, we demonstrate that LLDAS is an attainable treatment goal for children with SLE. In the Rotterdam cohort, all children achieved LLDAS within a median time of 6 months. We also demonstrate that the early introduction of immunosuppressants can limit the use of corticosteroids. Thus, the pursuit of LLDAS appears to be a feasible objective in cSLE and may potentially lead to improved long-term outcomes, including reduced organ damage and fewer disease flares.
While the clinical features of SLE provide valuable insights into disease activity and the occurrence of disease flares, there is a need for specific biological parameters that better reflect the underlying abnormal biological pathways. In Chapter 3.1, we demonstrate that a subset of patients with cSLE exhibits an elevated expression of the so-called IFN-I signature, which corresponds to increased levels of IFN-I proteins. Remarkably, in these patients, the expression of endoplasmic and cytosolic receptors responsible for IFN-I production appears to be elevated despite the use of various medications. We were able to inhibit the IFN-I signature by blocking the TBK-1 protein. This protein is part of the IFN-I signalling pathway. Therefore, TBK-1 may potentially serve as a novel therapeutic target in SLE in the future.
Nearly all SLE patients included in various scientific studies on the IFN-I signature to date were treated with one or more (immunosuppressive) medications. Interestingly, the majority of these patients still exhibited an elevated IFN-I signature despite these treatments. To investigate this, we established an in vitro model in Chapter 3.2 in which cells were activated through two IFN-I inducing routes, the endoplasmic and/or cytosolic pathways, followed by testing the effect of standard of care medications in SLE. As the tested medication appeared to have no effect on IFN-I production via the cytoplasmic pathways, the sustained production of IFN-I is likely occurring through these receptors.
Several studies suggest that the IFN-I signature is a potential biomarker for disease activity. However, multiple longitudinal studies have yielded conflicting results. Chapter 3.3 describes a comprehensive longitudinal cohort study. In this study, we assessed both the IFN-I signature and the concentration of IFN-I proteins. IFN-alpha2, one of the key IFN-I proteins, was measured using a highly sensitive Single-molecule assay called Simoa, which enables the measurement of very low concentrations of IFN-alpha2. Our results demonstrated that the IFN-I signature remained relatively stable over a three-year period and was not significantly associated with disease activity. However, we were able to show that the concentration of IFN-alpha2 in the blood, measured with Simoa, fluctuated over time and was associated with changes in disease activity. This highlights the importance of the method used to measure IFN-I activity for its applicability in the clinical setting as a biomarker for disease activity.
The IFN-I signature is not the only gene expression profile associated with SLE. Previous studies have demonstrated multiple gene expression profiles associated with cSLE. A combination of these profiles can be used to classify patients into more homogeneous groups based on their disease activity. However, the techniques used in the published landmark study are often too complex and costly for routine clinical practice. In Chapter 4.1, we translated these gene expression profiles into four simpler gene signatures that could be more easily applied in clinical practice. We demonstrated that a combination of these signatures could classify patients into groups with similar disease activity profiles. In a follow-up study, Chapter 4.2, these gene signatures were combined with specific proteins also associated with SLE. Subsequently, a computer model was used to classify patients into different groups based on these biological factors (gene expression and proteins). This approach resulted in three distinct clusters of patients with different disease activity profiles. Furthermore, we examined, through 40-color flow cytometry, whether the identified clusters were characterized by specific cell types in peripheral blood. Interestingly, multiple cell types were found to differ between these clusters. Together, these two studies emphasize the idea that future treatment decisions should not only be based on clinical characteristics but should also incorporate biological parameters.
In Chapter 5, we compare our findings with the existing literature. Several recent studies have demonstrated that achieving LLDAS is a feasible goal in cSLE. However, it is important to note that the current definition of LLDAS is tailored to adults. Thanks to the efforts of an international task force, definitions for children have now been established that still closely resemble those for adults, facilitating the comparability of future studies between childhood onset and adult onset SLE patients. While the results are predominantly positive for the T2T (Treat-to-Target) approach, there are still ideas to further refine this strategy. One of these concepts involves incorporating a measurable biological parameter into the T2T criteria. Ideally, this biomarker should be associated with disease activity, thereby enabling the achievement of the T2T strategy from a biological perspective. IFN-I appears promising in this regard, but candidates from multiple levels (genomics, transcriptomics, proteomics, etc.) seem to be emerging for this purpose. With the advent of new analysis methods, including artificial intelligence, research that combines biomarker-candidates from multiple levels appears to be even more relevant. However, the question remains whether this approach is feasible in practice, considering factors such as cost and technical complexity. Therefore, it remains the responsibility of researchers to develop techniques that are both cost-effective and feasible for clinical practice.
Bekijk ook deze proefschriften
Structure-Preserving Data-Driven Methods for Modeling Turbulent Flows
Molecular insights into the role of VRS5 in tillering and lateral spikelet development in barley
Gamma Knife Radiosurgery for Skull Base Tumors
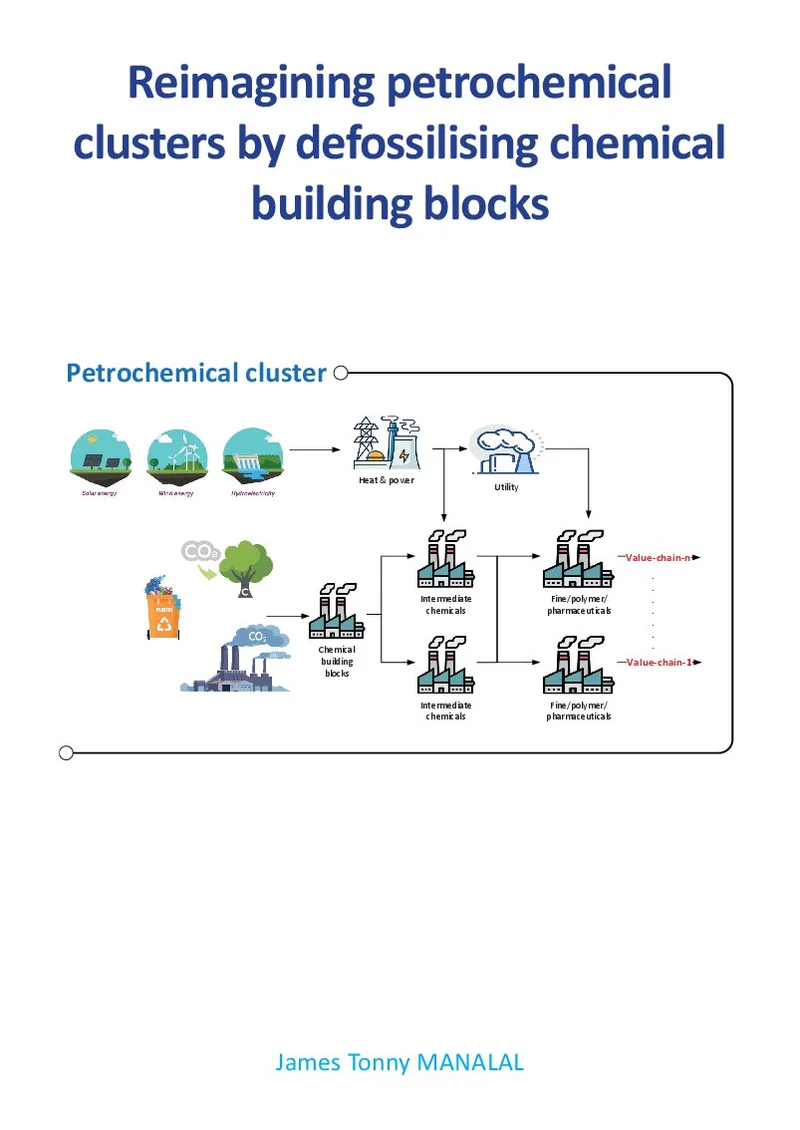
Reimagining petrochemical clusters by defossilising chemical building blocks
Microbial stabilization and protein functionality of plant-based liquids using pulsed electric fields
Wij drukken voor de volgende universiteiten