Deel dit project
Relating genomic and functional heterogeneity to clinical outcomes in epithelial ovarian cancer
Samenvatting
Kanker heeft een enorme impact op de wereldwijde gezondheidszorg. Eierstokkanker in het bijzonder is een ziekte met slechte uitkomsten. In tegenstelling tot andere kankersoorten is er bij eierstokkanker de afgelopen decennia weinig vooruitgang geboekt, ondanks meer gedetailleerde chirurgische behandelingen en het introduceren van nieuwe medicijnen. Van de vrouwen die de diagnose eierstokkanker krijgen leeft slechts 38% nog na 5 jaar.
Eierstokkanker is een heterogene ziekte, dat wil zeggen dat er veel verschillende uitingsvormen zijn. Op basis van weefselbeoordeling door de patholoog kan eierstokkanker onderverdeeld worden in een aantal verschillende histologische subtypen, ieder met specifieke eigenschappen. Een voorbeeld hiervan is het meest voorkomende en tevens ook meest agressieve subtype, ‘hooggradig sereus ovariumcarcinoom’ (HGSC). Door ontwikkelingen binnen het onderzoek naar DNA (erfelijk materiaal) is de afgelopen jaren aangetoond dat er niet alleen op weefselniveau maar ook op DNA-niveau uitgebreide verschillen bestaan tussen de verscheidene vormen van eierstokkanker. Dit betreft verschillen tussen de tumoren van diverse patiënten (ook bij patiënten die allen hetzelfde histologische subtype hebben) en het betreft verschillen tussen meerdere tumorlocaties van individuele patiënten.
Ondanks deze uitgebreide verschillen is de behandeling van uitgezaaide eierstokkanker zeer uniform. De eerstelijnsbehandeling bestaat uit een zogenoemde ‘debulking-operatie’ waarbij alle zichtbare tumor wordt verwijderd en platinum-bevattende chemotherapie. Hoewel de meeste patiënten initieel goed reageren op deze behandeling, komt bij de meerberheid van de patiënten de ziekte na verloop van tijd terug en wordt de kanker uiteindelijk resistent voor chemotherapie.
Laboratoriummodellen kunnen uitkomst bieden bij het verbeteren van behandelkeuzes voor individuele patiënten. Kankercellen van de patiënt kunnen buiten het lichaam getest worden op diverse medicijnen, alvorens een medicijn aan de patiënt wordt toegediend. De meest gebruikte laboratorium modellen voor onderzoek naar eierstokkanker zijn 2D-cellijnen en muizen. Beide modellen hebben specifieke voor- en nadelen. Twee-dimensionele cellijnen (monolagen) groeien erg snel en zijn daardoor geschikt voor het simultaan testen van vele medicijnen. Ze zijn echter slechts een simplistische weergave van de tumor, ze missen de meerlaagse celopbouw zoals deze in het lichaam aanwezig is. Muismodellen (muizen waar een tumor in getransplanteerd is) zijn daarentegen complexe kankermodellen die meer gelijkenis vertonen met kanker in het menselijk lichaam dan cellijnen. Daarnaast kunnen met behulp van muismodellen medicijnen in een levend organisme worden getest. Het nadeel van muismodellen is echter het gebruik van levende wezens. Tevens zijn deze modellen erg arbeidsintensief en daardoor ongeschikt voor grootschalige medicijnstudies.
Ongeveer tien jaar geleden is het organoïde model ontwikkeld. Organoïden (‘mini-orgaantjes’) groeien in tegenstelling tot traditionele 2D-cellijnen, in drie dimensies, en vormen hierdoor mini-orgaantjes of tumoren. De eerste organoïden waarover in 2009 werd gepubliceerd, waren gezonde darmcellen van muizen, al snel gevolgd door organoïden van menselijke darmcellen en darmkankercellen. Inmiddels zijn er organoïde modellen ontwikkeld van vele verschillende gezonde weefsels en kankersoorten (inclusief recentelijk van eierstokkanker) door het celkweekmedium aan te passen aan de uiteenlopende behoeften van de diverse cellen. In hoofdstuk 2 beschrijven we de opzet en de diverse toepassingen van een organoïde biobank van eierstokkanker. Dit hoofdstuk bevat een protocol waarmee cellen van eierstokkanker gedurende lange termijn als organoïden gekweekt kunnen worden. We hebben middels dit protocol 56 organoïden van 32 patiënten ontwikkeld, waarbij alle belangrijke subtypen van eierstokkanker vertegenwoordigd zijn. Alle samples zijn uitvoerig gekarakteriseerd, omdat het erg belangrijk is dat de gekweekte cellen in het laboratorium grote gelijkenis vertonen met de originele kankercellen. We hebben aangetoond dat organoïden van patiënten met eierstokkanker (patient-derived organoids, PDO’s) zowel op histopathologisch vlak als op DNA-niveau een goede weergave zijn van de originele kankercellen. Tevens zijn ze in het laboratorium stabiel gedurende een langere periode. De eerste medicijn testen op PDO’s vertoonden tevens subtype-specifieke responses. Van een individuele patiënt waarbij op meerdere momenten in de ziekte organoïden zijn gemaakt, vertoonden de PDO’s de transitie van chemotherapie gevoeligheid naar resistentie, overeenkomend met de transitie die de patiënt doormaakte. Verder werd het door het transplanteren van PDO’s in muizen mogelijk om tumoren van patiënten in een levend organisme te behandelen. Hoofdstuk 2 beschrijft ook de opzet en genetische modificatie van organoïden van gezond weefsel van eileiders en eierstok oppervlakte epitheel, waardoor tumorvorming kon worden nagebootst. Over het geheel genomen laten de resultaten van deze studie de potentie van PDO’s van eierstokkanker zien voor de wetenschap.
Alvorens PDO’s in de kliniek kunnen worden geïntroduceerd moet er vastgesteld worden dat de respons van PDO’s op medicijnen overeenkomt met hoe de patiënt op deze medicijnen reageert. In hoofdstuk 3 hebben we de laboratorium respons van PDO’s vergeleken met de klinische respons van patiënten, om vast te stellen of PDO’s gebruikt kunnen worden voor respons predictie. We hebben hiervoor zeven organoïden van vijf verschillende patiënten getest op de eerstelijns chemotherapie voor eierstokkanker, bestaande uit carboplatine en paclitaxel combinatietherapie. We lieten zien dat PDO’s representatief zijn voor de klinische respons, op basis van diverse klinische uitkomstmaten (histologisch, biochemisch en radiologisch). PDO’s van patiënten met de meest gunstige klinische respons vertoonden ook de beste reactie in het laboratorium, terwijl patiënten met minder goede PDO-uitslagen ook slechtere klinische uitkomsten hadden. Een andere belangrijke voorwaarde voor de introductie van PDO’s in de kliniek is een korte doorlooptijd. In hoofdstuk 3 laten we zien dat het mogelijk is vanaf het moment van weefsel biopt binnen drie weken een organoïde te laten groeien en een medicijn uitslag te hebben. Dit resultaat komt overeen met recente publicaties van andere onderzoeksgroepen.
Hoewel er veel onderzoek is gedaan naar de heterogeniteit van eierstokkanker op DNA-niveau, is er minder bekend over functionele heterogeniteit. In hoofdstuk 3 vergelijken we de medicijn respons van verschillende patiënten, voor zowel standaard chemotherapeutica als gerichte therapieën. PDO’s vertoonden zowel verschillen in medicijnrespons tussen patiënten alsmede binnen patiënten (dus tussen PDO’s van verschillende tumorlocaties van een individuele patiënt). Een deel van deze verschillen konden we verklaren door geobserveerde variaties in het DNA. Een belangrijke notie is dan ook dat een enkel biopt mogelijk niet voldoende is om een goede inschatting te maken voor de verwachte medicijn respons bij een individuele patiënt.
Er is een vervolgstudie nodig om de aangetoonde relatie tussen de laboratorium resultaten en de klinische resultaten te versterken. Hoewel we in hoofdstuk 3 een reeds een correlatie hebben aangetoond was de studiepopulatie hier klein en werd de klinische respons enkel gedefinieerd door middel van directe uitkomsten en niet door lange termijn uitkomsten. Hoofdstuk 4 beschrijft een studieprotocol voor een prospectieve observationele cohortstudie. Het doel van deze studie is het vaststellen van de voorspellende waarde van PDO’s voor lange termijn klinische respons (gedefinieerd als progressie vrije overleving). Daarnaast willen we in deze studie een afkapwaarde vaststellen voor slechte responders op basis van de organoïde medicijntest, zodat patiënten met een slechte prognose in de toekomst eerder kunnen worden geïdentificeerd. De uitkomsten van deze studie zouden PDO’s dichterbij de kliniek kunnen brengen. Aangezien het percentage van succesvolle organoïde kweken nog beperkt is voor het HGSC-subtype adviseren wij nog een aanvullende medium optimalisatie stap voordat de studie zoals beschreven in hoofdstuk 4 van start gaat.
Waar in de voorgaande hoofdstukken whole genome sequencing (WGS) met name ingezet is om organoïden te karakteriseren, focussen we in hoofdstuk 5 op deze techniek. We beschrijven hier de analyse van WGS-data van een grote groep van patiënten met uitgezaaide eierstokkanker. Momenteel is de behandelkeuze met name gebaseerd op het histologische subtype, ziektestadium, tijd tot de terugkeer van ziekte en eerdere respons op platinum-bevattende chemotherapie. In dit hoofdstuk bestuderen we de relatie tussen WGS-data en klinische (respons) data van patiënten met eierstokkanker. Met als doel om op basis van DNA-informatie een meer gepersonaliseerde behandeling te creëren. Hiervoor hebben we met computer analyses de WGS-data ‘automatisch gesorteerd’ waardoor data van patiënten die op DNA-niveau het meest op elkaar lijken in dezelfde groep eindigen. We laten in hoofdstuk 5 zien dat deze methode specifieke groepen creëert, ieder met specifieke respons percentages en prognoses. Hierdoor is het mogelijk om tumoren te classificeren buiten de traditionele histopathologische criteria om. Daarnaast werden bij een analyse gericht op het identificeren van DNA-veranderingen waar een gerichte behandeling voor bestaat, interessante behandelopties gevonden. Echter, de meeste van deze behandelopties betreffen medicijnen die nog niet regulier beschikbaar zijn voor patiënten met eierstokkanker, of waarvan de werkzaamheid nog niet met voldoende zekerheid is aangetoond. Opmerkelijk genoeg vertoonde patiënten in het cluster met de slechtste prognose het vaakst een DNA-verandering waar een indicatie voor een experimentele gerichte therapie voor bestaat.
Concluderend heeft het werk in dit proefschrift geresulteerd in de ontwikkeling van een nieuw preklinisch PDO modelsysteem voor eierstokkanker, dat representatief is voor de originele tumor, geschikt is voor het screenen van medicijnen en tevens de complexiteit en heterogeniteit van eierstokkanker weet te vatten, zowel ten aanzien van de verschillen tussen patiënten als binnen patiënten. PDO’s zijn waardevolle modelsystemen die de potentie hebben om inzicht te verkrijgen in medicijn respons van individuele patiënten met eierstokken, complementair aan genetische testen. Een vervolgstudie is noodzakelijk waarin de correlatie tussen PDO medicijn respons en lange termijn klinische respons wordt aangetoond. Verder kunnen we door middel van WGS ons inzicht in medicijn respons vergroten en potentieel de keuze voor de juiste behandeling voor patiënten met uitgezaaide eierstokkanker verbeteren. Door het complexe en heterogene karakter van eierstokkanker te onderkennen en een meer geïndividualiseerde aanpak na te streven is het mogelijk om uiteindelijk de vooruitzichten voor patiënten met eierstokkanker te verbeteren.
Bekijk ook deze proefschriften
Structure-Preserving Data-Driven Methods for Modeling Turbulent Flows
Molecular insights into the role of VRS5 in tillering and lateral spikelet development in barley
Gamma Knife Radiosurgery for Skull Base Tumors
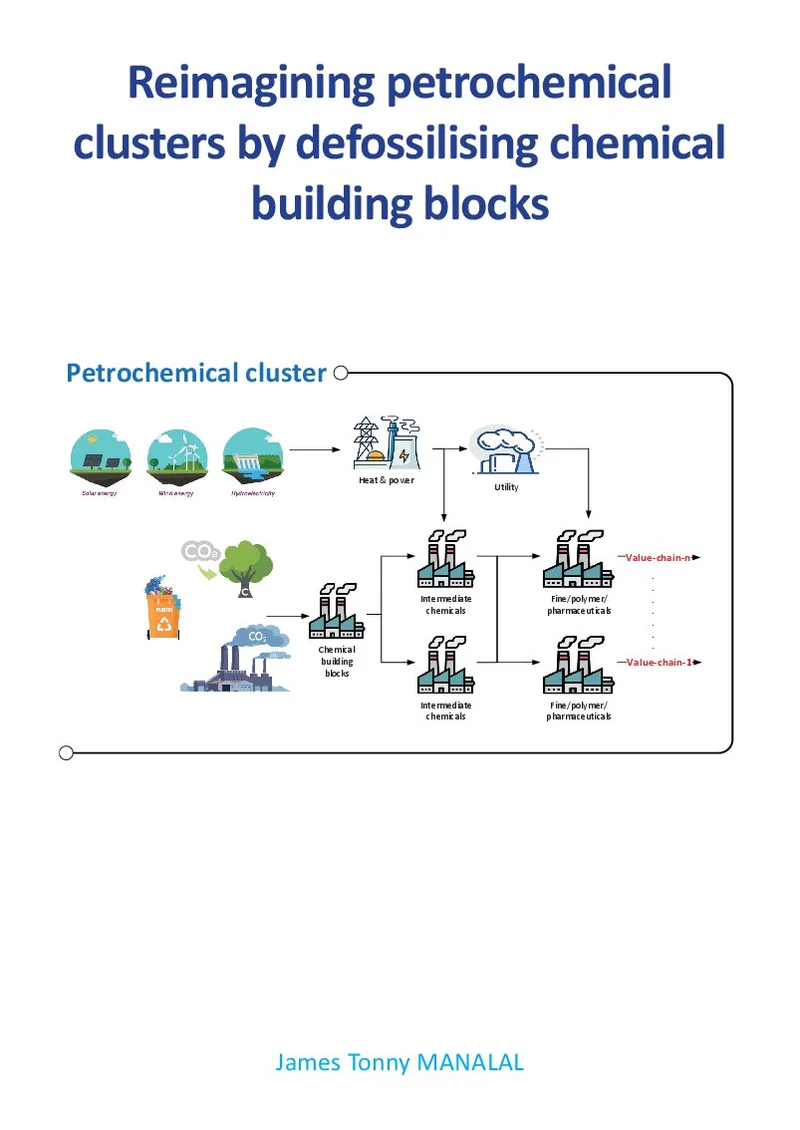
Reimagining petrochemical clusters by defossilising chemical building blocks
Microbial stabilization and protein functionality of plant-based liquids using pulsed electric fields
Wij drukken voor de volgende universiteiten